Expo
ver canal
ver canal
ver canal
ver canal
ver canal
ver canal
ver canal
ver canal
Química Clínica
HematologíaInmunologíaMicrobiologíaPatologíaTecnologíaIndustria
Eventos
Webinars

- Marcadores de cáncer de próstata basados en composición química de calcificaciones aceleran detección
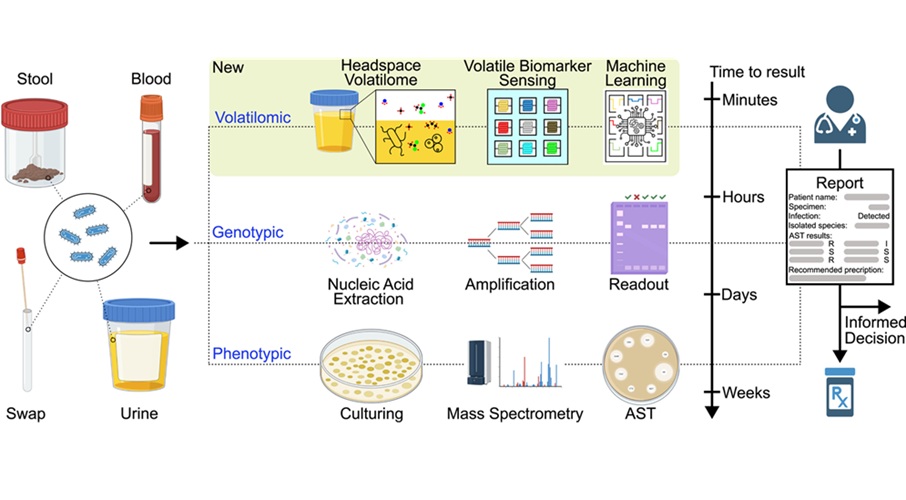
- Prueba de aliento ayuda a detectar cánceres de sangre
- Sensores de gas alimentados por ML detectan patógenos y RAM en POC
- Tecnología de detección de cáncer en saliva elimina preparación compleja de muestras
- Hisopos cutáneos podrían detectar Parkinson años antes de que aparezcan síntomas
- Nuevo análisis podría cambiar pruebas para enfermedad de Lyme
- Análisis sanguíneo en primer trimestre predice diabetes gestacional
- Firma de ADN microbiano en plasma sanguíneo diferencia dos cánceres de hígado
- Sencilla prueba de fluidos corporales ofrece detección rentable y altamente sensible del Alzheimer
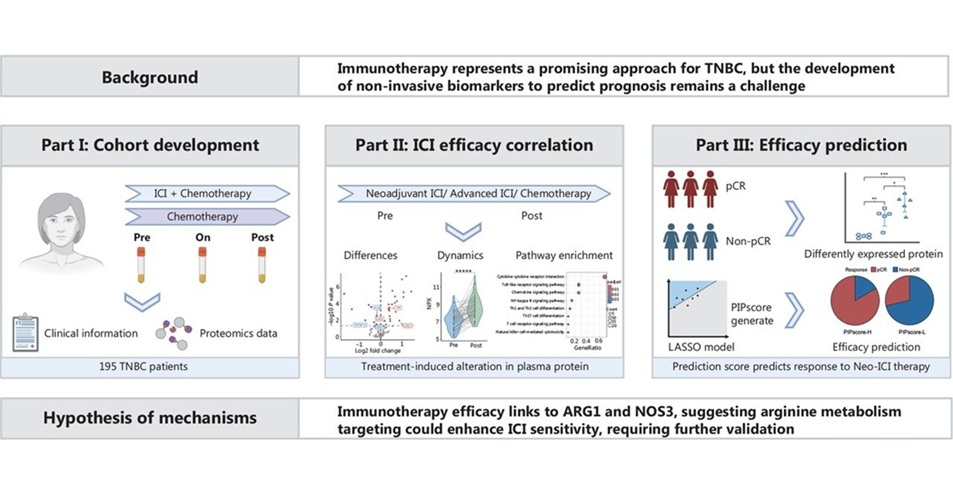
- Nuevo enfoque identifica pacientes con cáncer mamario resistente al tratamiento
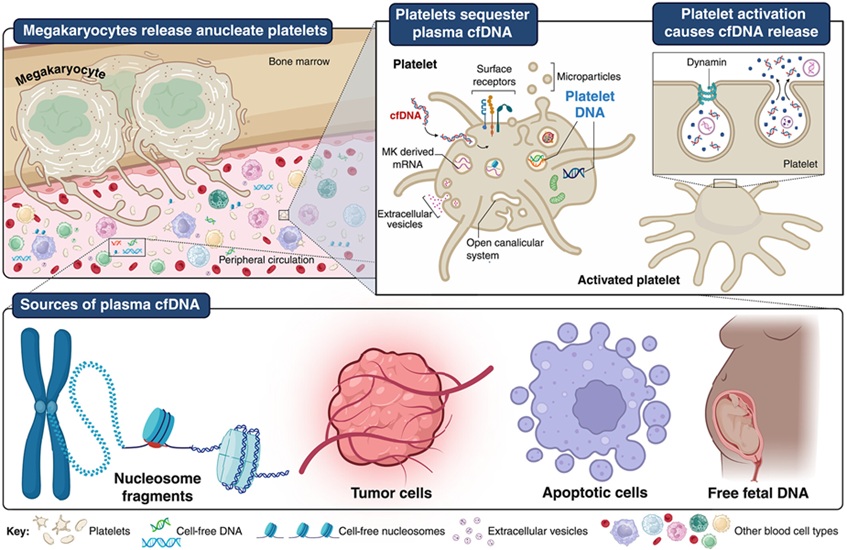
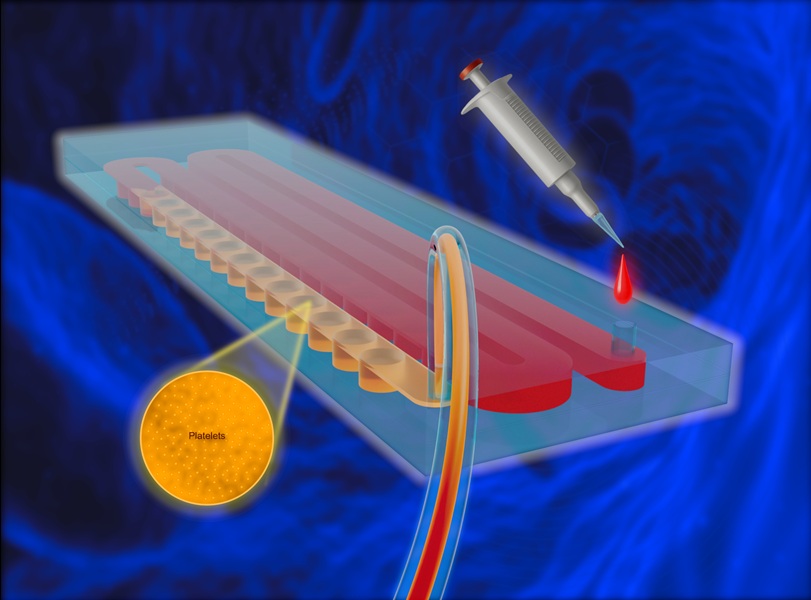
- Dispositivo portátil desechable obtiene plasma rico en plaquetas sin equipos complejos
- Prueba de cartucho desechable ofrece resultados de hemograma rápidos y precisos
- Primera prueba de monitorización de heparina POC proporciona resultados rápidos
- Nuevo sistema de puntuación predice riesgo de cáncer a partir de un trastorno sanguíneo común
- Prueba prenatal no invasiva para determinar estado RhD del feto es 100 % precisa
- Pruebas genéticas simples podrían predecir éxito del tratamiento de esclerosis múltiple
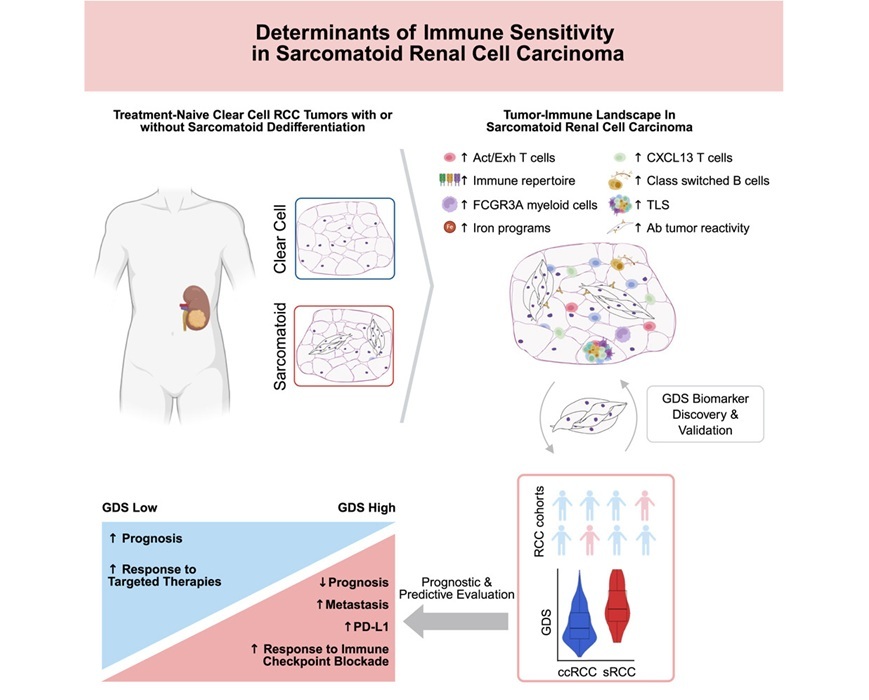
- Nueva firma genética predice respuesta a inmunoterapia en cánceres renales avanzados
- Nueva tecnología descifra comunicación entre células inmunitarias para predecir respuesta a inmunoterapia
- IA predice con precisión respuesta de inhibidores de puntos de control inmunitario y tumor MSI
- Herramienta de precisión predice fracaso del tratamiento de inmunoterapia en melanoma
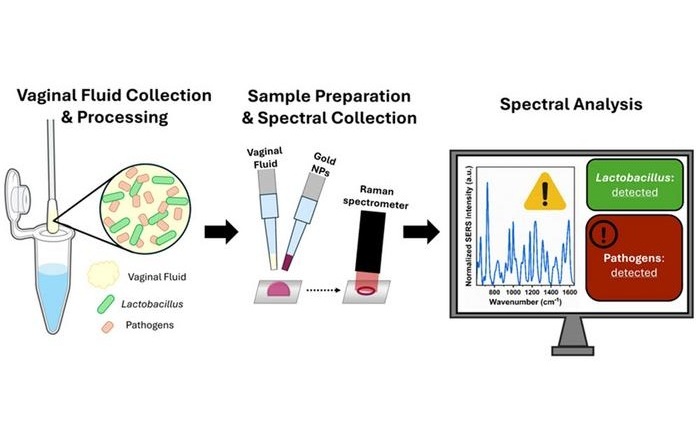
- Espectroscopia portátil detecta de forma rápida y no invasiva bacterias en fluido vaginal
- Prueba de saliva basada en CRISPR detecta tuberculosis en esputo
- Análisis de orina diagnostica infección pulmonar común en personas inmunodeprimidas
- Prueba salival detecta riesgos microbianos relacionados con implantes
- Nueva plataforma aprovecha IA y computación cuántica para predecir resistencia a antimicrobianos de Salmonella
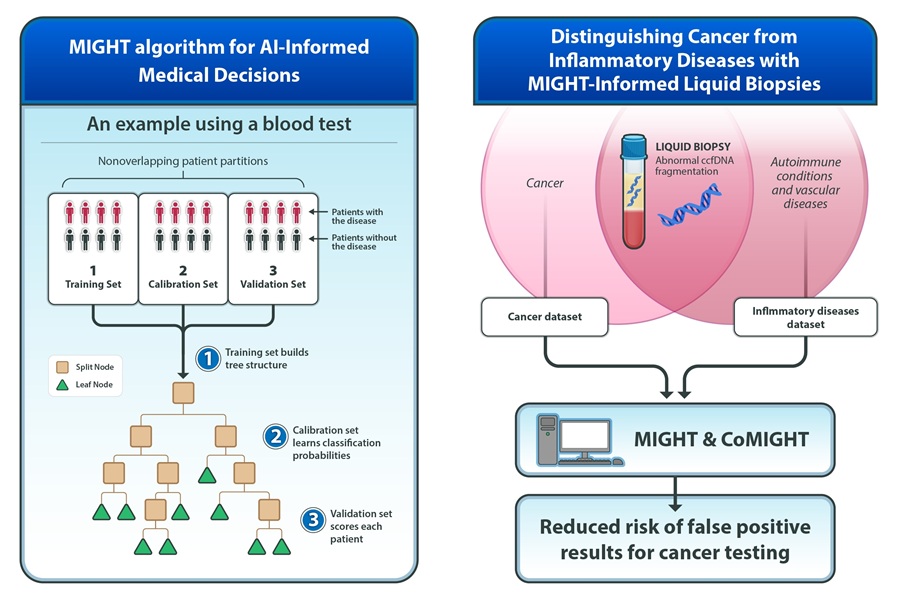
- Nuevo método mejora fiabilidad de la IA con aplicaciones en diagnóstico médico
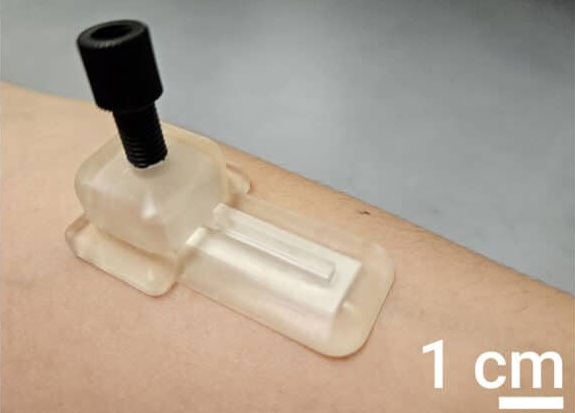
- Parche de microagujas autoalimentado recolecta muestras de biomarcadores sin extraer sangre
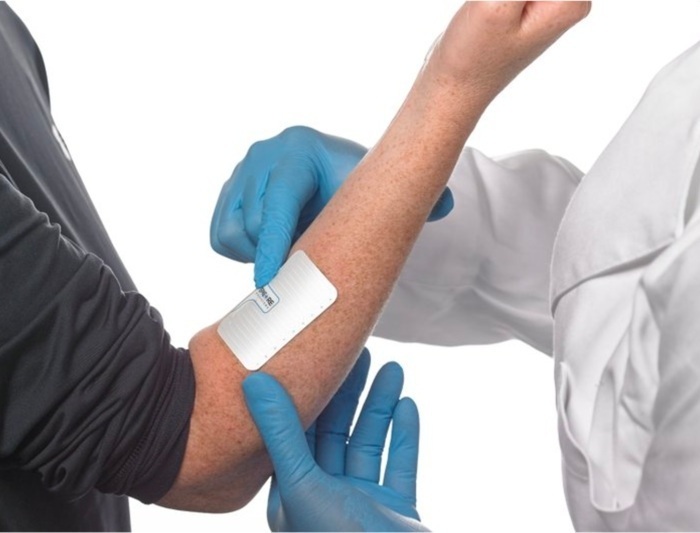
- Parche cutáneo detecta biomarcadores en líquido intersticial sin extracción de sangre
- Prueba de saliva portátil detecta cáncer mamario con precisión
- Algoritmos avanzados de IA permiten detección temprana del cáncer prostático
- OMS publica guía actualizada sobre diagnóstico de tuberculosis
- Colaboración pionera transforma diagnóstico e investigación del cáncer pediátrico
- Bio-Techne vende Exosome Diagnostics para reposicionar su cartera de productos
- Nuevas directrices clínicas recomiendan el uso de análisis de sangre en lugar de escáneres cerebrales para diagnóstico del Alzheimer
- IFCC WorldLab 2026 se celebrará en India del 25 al 29 de octubre
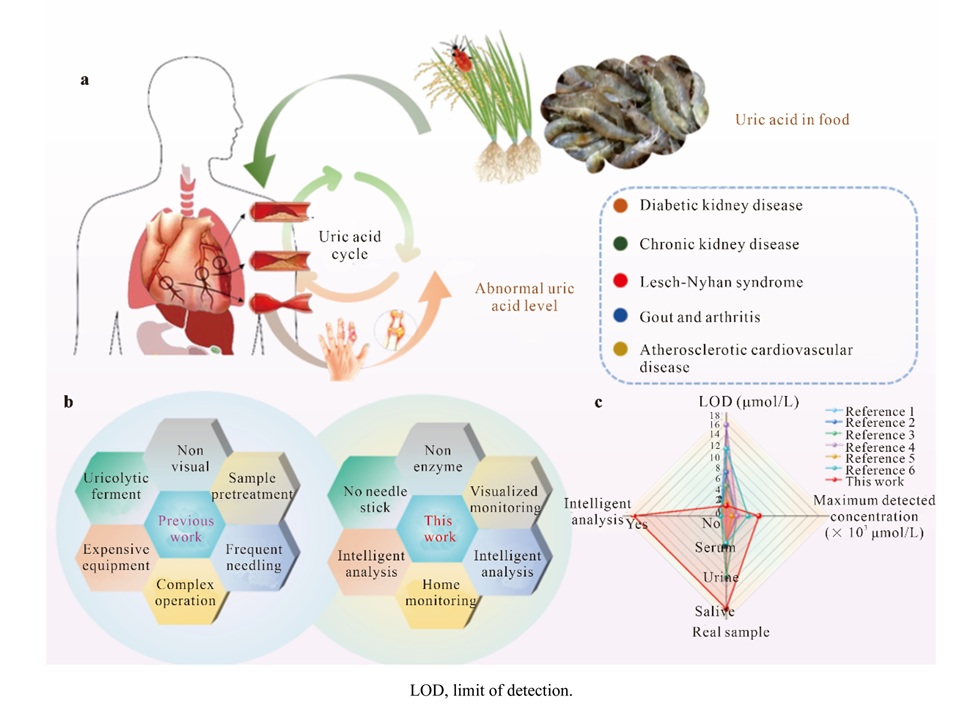
- Nueva tecnología acelera diagnóstico de enfermedad renal diabética
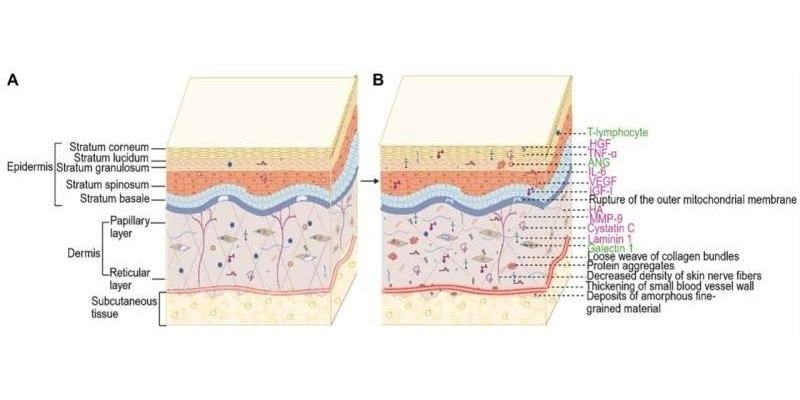
- Biomarcadores cutáneos para diagnóstico precoz de esclerosis lateral amiotrófica
- Herramientas de IA analizan enfermedad renal a nivel celular para ayudar a adaptar tratamientos
- Sistema totalmente automatizado transforma manejo preanalítico de muestras de orina
- Prueba con IA ofrece análisis cuantitativo automatizado de evaluación de fibrosis

 Expo
Expo
- Marcadores de cáncer de próstata basados en composición química de calcificaciones aceleran detección
- Prueba de aliento ayuda a detectar cánceres de sangre
- Sensores de gas alimentados por ML detectan patógenos y RAM en POC
- Tecnología de detección de cáncer en saliva elimina preparación compleja de muestras
- Hisopos cutáneos podrían detectar Parkinson años antes de que aparezcan síntomas
- Nuevo análisis podría cambiar pruebas para enfermedad de Lyme
- Análisis sanguíneo en primer trimestre predice diabetes gestacional
- Firma de ADN microbiano en plasma sanguíneo diferencia dos cánceres de hígado
- Sencilla prueba de fluidos corporales ofrece detección rentable y altamente sensible del Alzheimer
- Nuevo enfoque identifica pacientes con cáncer mamario resistente al tratamiento
- Dispositivo portátil desechable obtiene plasma rico en plaquetas sin equipos complejos
- Prueba de cartucho desechable ofrece resultados de hemograma rápidos y precisos
- Primera prueba de monitorización de heparina POC proporciona resultados rápidos
- Nuevo sistema de puntuación predice riesgo de cáncer a partir de un trastorno sanguíneo común
- Prueba prenatal no invasiva para determinar estado RhD del feto es 100 % precisa
- Pruebas genéticas simples podrían predecir éxito del tratamiento de esclerosis múltiple
- Nueva firma genética predice respuesta a inmunoterapia en cánceres renales avanzados
- Nueva tecnología descifra comunicación entre células inmunitarias para predecir respuesta a inmunoterapia
- IA predice con precisión respuesta de inhibidores de puntos de control inmunitario y tumor MSI
- Herramienta de precisión predice fracaso del tratamiento de inmunoterapia en melanoma
- Espectroscopia portátil detecta de forma rápida y no invasiva bacterias en fluido vaginal
- Prueba de saliva basada en CRISPR detecta tuberculosis en esputo
- Análisis de orina diagnostica infección pulmonar común en personas inmunodeprimidas
- Prueba salival detecta riesgos microbianos relacionados con implantes
- Nueva plataforma aprovecha IA y computación cuántica para predecir resistencia a antimicrobianos de Salmonella
- Nuevo método mejora fiabilidad de la IA con aplicaciones en diagnóstico médico
- Parche de microagujas autoalimentado recolecta muestras de biomarcadores sin extraer sangre
- Parche cutáneo detecta biomarcadores en líquido intersticial sin extracción de sangre
- Prueba de saliva portátil detecta cáncer mamario con precisión
- Algoritmos avanzados de IA permiten detección temprana del cáncer prostático
- OMS publica guía actualizada sobre diagnóstico de tuberculosis
- Colaboración pionera transforma diagnóstico e investigación del cáncer pediátrico
- Bio-Techne vende Exosome Diagnostics para reposicionar su cartera de productos
- Nuevas directrices clínicas recomiendan el uso de análisis de sangre en lugar de escáneres cerebrales para diagnóstico del Alzheimer
- IFCC WorldLab 2026 se celebrará en India del 25 al 29 de octubre
- Encuentran etiologías de COVID prolongada en muestras de sangre con infección aguda
- Dispositivo novedoso detecta anticuerpos contra la COVID-19 en cinco minutos
- Prueba para COVID-19 mediante CRISPR detecta SARS-CoV-2 en 30 minutos usando tijeras genéticas
- Asocian disbiosis del microbioma intestinal con la COVID-19
- Validan prueba rápida novedosa de antígeno para el SARS-CoV-2 con respecto a su exactitud diagnóstica
- Nueva tecnología acelera diagnóstico de enfermedad renal diabética
- Biomarcadores cutáneos para diagnóstico precoz de esclerosis lateral amiotrófica
- Herramientas de IA analizan enfermedad renal a nivel celular para ayudar a adaptar tratamientos
- Sistema totalmente automatizado transforma manejo preanalítico de muestras de orina
- Prueba con IA ofrece análisis cuantitativo automatizado de evaluación de fibrosis