Expo
ver canal
ver canal
ver canal
ver canal
ver canal
ver canal
ver canal
ver canal
Química ClínicaDiagnóstico MolecularHematologíaInmunologíaMicrobiologíaPatología
Industria
Eventos
Webinars

- Espectroscopia Raman portátil ofrece diagnóstico rentable de enfermedad renal en POC
- Nanopartículas de oro mejoran precisión del diagnóstico de cáncer ovárico
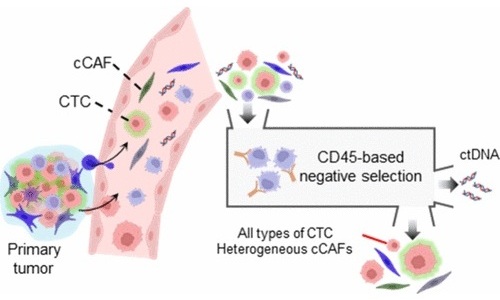
- Tecnología de aislamiento celular simultáneo mejora precisión del diagnóstico del cáncer
- Sencilla prueba capilar no invasiva podría acelerar diagnóstico de ELA
- Prueba de saliva detecta niveles elevados de ácido úrico sin necesidad de extraer sangre
- Biomarcadores sanguíneos duales mejoran precisión del diagnóstico de ELA
- Prueba automatizada distingue dengue de enfermedades que causan fiebre aguda en 18 minutos
- Prueba de troponina I de alta sensibilidad diagnóstica infarto de miocardio
- Pruebas rápidas y económicas del Alzheimer podrían detectar enfermedad en etapas tempranas
- Investigación adicional de pruebas FISH negativas para carcinoma de células renales mejora precisión diagnóstica
- Pruebas viscoelásticas podrían mejorar tratamiento de hemorragia materna
- Modelo mide exposición a radiación en sangre para tratamientos precisos contra cáncer
- Las plaquetas podrían mejorar detección temprana y mínimamente invasiva del cáncer
- Dispositivo portátil desechable obtiene plasma rico en plaquetas sin equipos complejos
- Prueba de cartucho desechable ofrece resultados de hemograma rápidos y precisos
- Modelo de biopsia líquida en sangre analiza eficacia de inmunoterapia
- Genes característicos predicen expansión de células T en inmunoterapia
- Diagnóstico por microscopio molecular evalúa rechazo del trasplante de pulmón
- Análisis sanguíneo detecta resistencia al tratamiento en cáncer ovárico seroso de alto grado
- Sonda luminiscente mide actividad de células inmunitarias en tiempo real
- Paneles entéricos de alto rendimiento detectan múltiples infecciones bacterianas gastrointestinales
- Prueba rápida no invasiva utiliza huella de azúcar para detectar infecciones por hongos
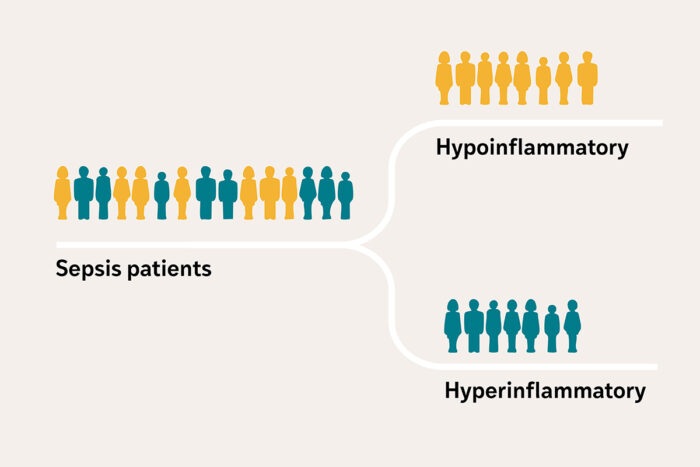
- Dispositivo de diagnóstico rápido de sepsis para atención crítica personalizada a pacientes de UCI
- Plataforma microfluídica evalúa función de neutrófilos en pacientes con sepsis
- Nuevo método diagnóstico confirma sepsis de forma más temprana
- Biosensor portátil diagnostica trastornos psiquiátricos mediante muestras de saliva
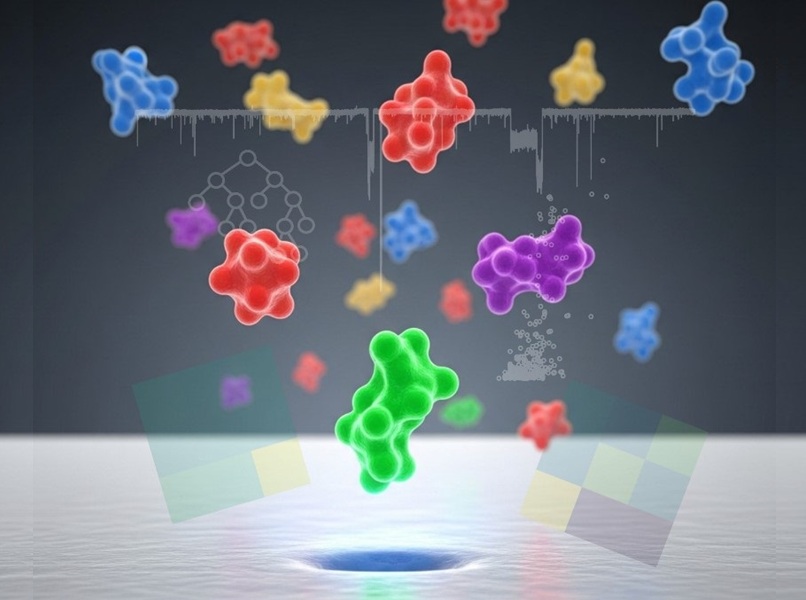
- Dispositivo de clasificación celular utiliza levitación electromagnética para dirigir con precisión movimiento celular
- Plataforma GPU integrada permite análisis rápido de sangre para diagnósticos en POC
- Prueba de biosensor viral detecta simultáneamente hepatitis y VIH
- Dispositivo acustofluídico transforma diagnóstico basado en VEp POC
- Qiagen adquiere empresa de ómica unicelular Parse Biosciences
- Puritan Medical Products presenta sus innovaciones en AMP2025 en Boston
- Advanced Instruments se fusionó como Nova Biomedical
- Bio-Rad y Biodesix se asocian para desarrollar ensayos de PCR digital de gotas complejos
- Hologic será adquirida por Blackstone y TPG
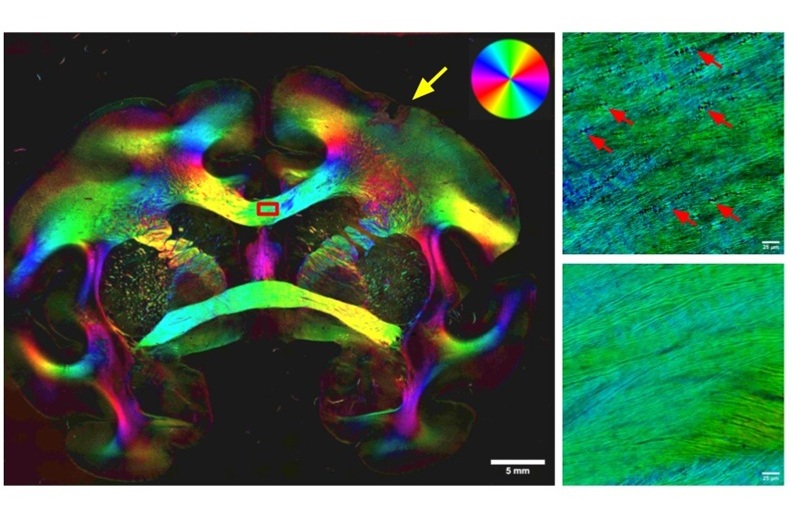
- Técnica de imagen de alta sensibilidad detecta daño en mielina
- Herramienta de mapeo del genoma 3D mejora diagnóstico y tratamiento de enfermedades genéticas
- Nueva herramienta de análisis molecular mejora diagnóstico de enfermedades
- Lágrimas ofrecen alternativa no invasiva para diagnósticar enfermedades neurodegenerativas
- Método impulsado por IA combina datos sanguíneos para medir con precisión edad biológica

 Expo
Expo
- Espectroscopia Raman portátil ofrece diagnóstico rentable de enfermedad renal en POC
- Nanopartículas de oro mejoran precisión del diagnóstico de cáncer ovárico
- Tecnología de aislamiento celular simultáneo mejora precisión del diagnóstico del cáncer
- Sencilla prueba capilar no invasiva podría acelerar diagnóstico de ELA
- Prueba de saliva detecta niveles elevados de ácido úrico sin necesidad de extraer sangre
- Biomarcadores sanguíneos duales mejoran precisión del diagnóstico de ELA
- Prueba automatizada distingue dengue de enfermedades que causan fiebre aguda en 18 minutos
- Prueba de troponina I de alta sensibilidad diagnóstica infarto de miocardio
- Pruebas rápidas y económicas del Alzheimer podrían detectar enfermedad en etapas tempranas
- Investigación adicional de pruebas FISH negativas para carcinoma de células renales mejora precisión diagnóstica
- Pruebas viscoelásticas podrían mejorar tratamiento de hemorragia materna
- Modelo mide exposición a radiación en sangre para tratamientos precisos contra cáncer
- Las plaquetas podrían mejorar detección temprana y mínimamente invasiva del cáncer
- Dispositivo portátil desechable obtiene plasma rico en plaquetas sin equipos complejos
- Prueba de cartucho desechable ofrece resultados de hemograma rápidos y precisos
- Modelo de biopsia líquida en sangre analiza eficacia de inmunoterapia
- Genes característicos predicen expansión de células T en inmunoterapia
- Diagnóstico por microscopio molecular evalúa rechazo del trasplante de pulmón
- Análisis sanguíneo detecta resistencia al tratamiento en cáncer ovárico seroso de alto grado
- Sonda luminiscente mide actividad de células inmunitarias en tiempo real
- Paneles entéricos de alto rendimiento detectan múltiples infecciones bacterianas gastrointestinales
- Prueba rápida no invasiva utiliza huella de azúcar para detectar infecciones por hongos
- Dispositivo de diagnóstico rápido de sepsis para atención crítica personalizada a pacientes de UCI
- Plataforma microfluídica evalúa función de neutrófilos en pacientes con sepsis
- Nuevo método diagnóstico confirma sepsis de forma más temprana
- Biosensor portátil diagnostica trastornos psiquiátricos mediante muestras de saliva
- Dispositivo de clasificación celular utiliza levitación electromagnética para dirigir con precisión movimiento celular
- Plataforma GPU integrada permite análisis rápido de sangre para diagnósticos en POC
- Prueba de biosensor viral detecta simultáneamente hepatitis y VIH
- Dispositivo acustofluídico transforma diagnóstico basado en VEp POC
- Qiagen adquiere empresa de ómica unicelular Parse Biosciences
- Puritan Medical Products presenta sus innovaciones en AMP2025 en Boston
- Advanced Instruments se fusionó como Nova Biomedical
- Bio-Rad y Biodesix se asocian para desarrollar ensayos de PCR digital de gotas complejos
- Hologic será adquirida por Blackstone y TPG
- Encuentran etiologías de COVID prolongada en muestras de sangre con infección aguda
- Dispositivo novedoso detecta anticuerpos contra la COVID-19 en cinco minutos
- Prueba para COVID-19 mediante CRISPR detecta SARS-CoV-2 en 30 minutos usando tijeras genéticas
- Asocian disbiosis del microbioma intestinal con la COVID-19
- Validan prueba rápida novedosa de antígeno para el SARS-CoV-2 con respecto a su exactitud diagnóstica
- Técnica de imagen de alta sensibilidad detecta daño en mielina
- Herramienta de mapeo del genoma 3D mejora diagnóstico y tratamiento de enfermedades genéticas
- Nueva herramienta de análisis molecular mejora diagnóstico de enfermedades
- Lágrimas ofrecen alternativa no invasiva para diagnósticar enfermedades neurodegenerativas
- Método impulsado por IA combina datos sanguíneos para medir con precisión edad biológica