Expo
ver canal
ver canal
ver canal
ver canal
ver canal
ver canal
ver canal
ver canal
Química ClínicaDiagnóstico MolecularHematologíaInmunologíaMicrobiologíaPatologíaTecnología
Eventos
Webinars

- Un estudio revela que la medición de ApoB es más eficaz que LDL para guiar la terapia lipídica
- Prueba en el punto de atención basada en IA cuantifica múltiples biomarcadores cardíacos
- Prueba de metabolitos en sangre detecta deterioro cognitivo temprano
- Analizadores automatizados de nueva generación aumentan el rendimiento en química clínica y pruebas de electrolitos
- Análisis de sangre basado en IA detecta múltiples trastornos cerebrales a partir de una sola muestra
- Las interacciones genéticas huésped-virus impulsan el riesgo de cáncer nasofaríngeo
- Biochip con IA detecta biomarcadores de microARN en minutos
- Plataforma de secuenciación de ARN de lectura larga mejora el diagnóstico de enfermedades raras
- Estudio confirma el esófago de Barrett como precursor del cáncer esofágico
- Ensayo ultrasensible revela tuberculosis previamente no detectada en pacientes hospitalarios
- Nuevo ensayo de función plaquetaria permite monitorizar la terapia antiplaquetaria
- Herramienta pronóstica guía el tratamiento personalizado en cáncer hematológico raro
- Plataforma abierta de multiómica identifica subtipos pronósticos en cánceres hematológicos
- Prueba rápida en cartuchos busca ampliar acceso al diagnóstico de trastornos de hemoglobina
- Nuevas directrices buscan mejorar diagnóstico de amiloidosis AL
- Prueba de anticuerpos en sangre identifica tuberculosis activa y distingue la infección latente
- Identifican una vía inflamatoria que impulsa la resistencia a la inmunoterapia en el cáncer de vejiga
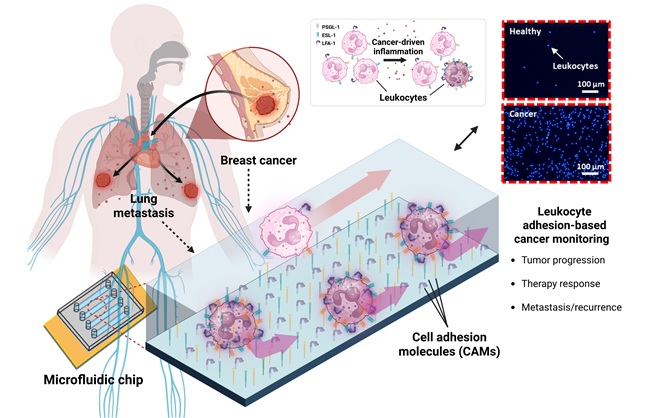
- Chip microfluídico detecta la recurrencia del cáncer a partir de señales de respuesta inmunitaria
- Firmas de mutación del cáncer mejoran la predicción de la respuesta a inmunoterapia
- Firma inmunitaria identificada en miastenia gravis resistente al tratamiento
- Panel sindrómico permite identificación rápida de infecciones del torrente sanguíneo
- Nuevo objetivo bacteriano identificado para la detección temprana del noma
- Prueba rápida de orina acelera la selección de antibióticos para infecciones del tracto urinario
- El análisis genómico vincula cepas estreptocócicas emergentes con infecciones específicas
- La OMS respalda las pruebas rápidas en el punto de atención para mejorar la detección de tuberculosis
- Sistema integrado optimiza el flujo de trabajo preanalítico para pruebas moleculares
- Prueba de esputo no invasiva detecta el cáncer de pulmón en etapa temprana
- Nueva herramienta de IA permite seleccionar rápidamente el tratamiento en leucemia pediátrica
- Diseño innovador de espectrometría de masas podría permitir la detección de abundancias ultrabajas
- Biosensor rápido detecta la sensibilidad a fármacos en tumores de mama
- Beckman Coulter obtiene el marcado CE para un ensayo rápido que distingue infecciones bacterianas de virales
- Takara Bio USA y Hamilton se asocian para automatizar la preparación de bibliotecas NGS
- Integrated DNA Technologies se expande al ámbito del diagnóstico clínico
- Agilent Technologies adquiere la empresa de diagnóstico patológico Biocare Medical
- Cepheid se une a iniciativa del CDC para fortalecer pruebas detección de pandemias
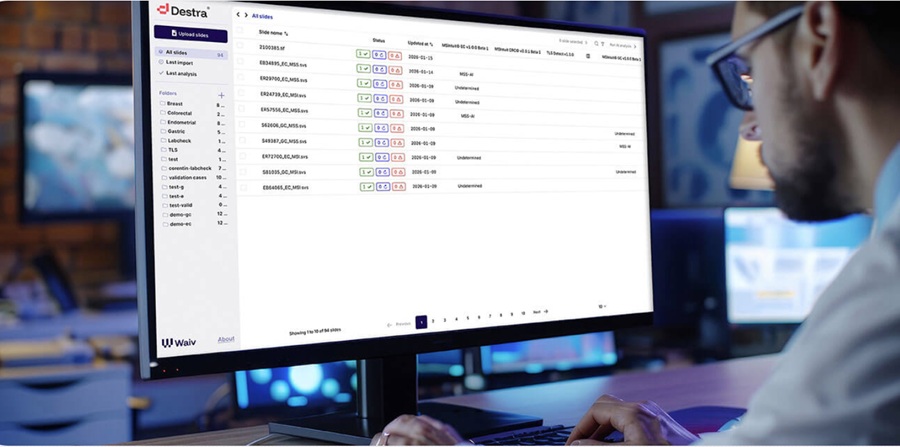
- La IA ayuda a los clínicos con informes complejos de patología oncológica
- Herramienta de IA predice respuesta a la quimioterapia en cáncer de pulmón de células pequeñas
- Biomarcador tumoral específico predice respuesta a inmunoterapia neoadyuvante en cáncer gástrico
- Nueva prueba de IA predice resultados de quimioterapia específicos para cada paciente con cáncer de mama
- Modelo patológico basado en IA guía las decisiones de quimioterapia en cáncer de mama.

 Expo
Expo
- Un estudio revela que la medición de ApoB es más eficaz que LDL para guiar la terapia lipídica
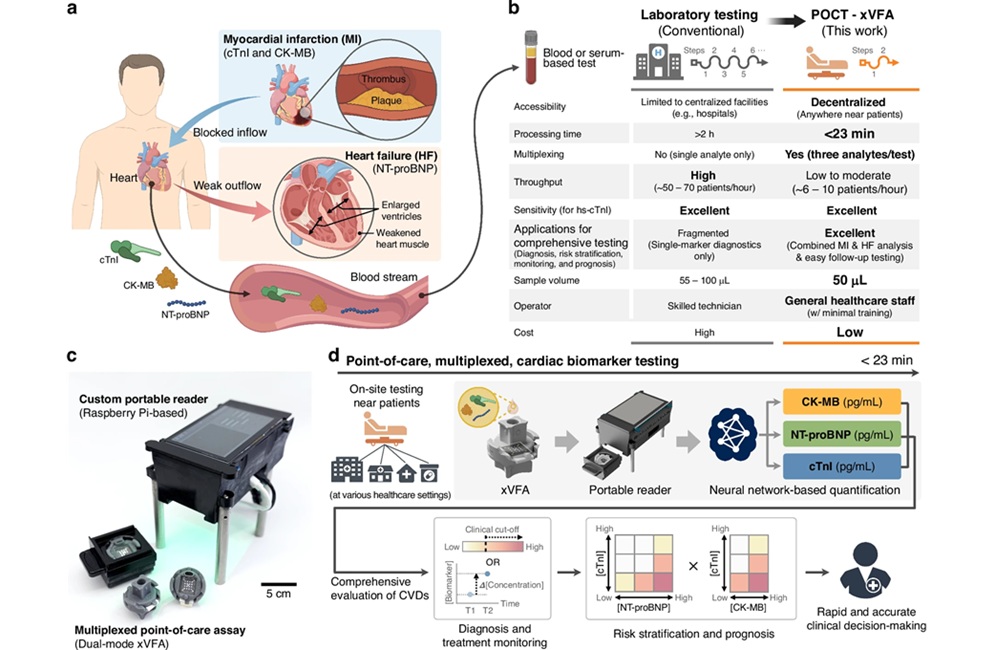
- Prueba en el punto de atención basada en IA cuantifica múltiples biomarcadores cardíacos
- Prueba de metabolitos en sangre detecta deterioro cognitivo temprano
- Analizadores automatizados de nueva generación aumentan el rendimiento en química clínica y pruebas de electrolitos
- Análisis de sangre basado en IA detecta múltiples trastornos cerebrales a partir de una sola muestra
- Las interacciones genéticas huésped-virus impulsan el riesgo de cáncer nasofaríngeo
- Biochip con IA detecta biomarcadores de microARN en minutos
- Plataforma de secuenciación de ARN de lectura larga mejora el diagnóstico de enfermedades raras
- Estudio confirma el esófago de Barrett como precursor del cáncer esofágico
- Ensayo ultrasensible revela tuberculosis previamente no detectada en pacientes hospitalarios
- Nuevo ensayo de función plaquetaria permite monitorizar la terapia antiplaquetaria
- Herramienta pronóstica guía el tratamiento personalizado en cáncer hematológico raro
- Plataforma abierta de multiómica identifica subtipos pronósticos en cánceres hematológicos
- Prueba rápida en cartuchos busca ampliar acceso al diagnóstico de trastornos de hemoglobina
- Nuevas directrices buscan mejorar diagnóstico de amiloidosis AL
- Prueba de anticuerpos en sangre identifica tuberculosis activa y distingue la infección latente
- Identifican una vía inflamatoria que impulsa la resistencia a la inmunoterapia en el cáncer de vejiga
- Chip microfluídico detecta la recurrencia del cáncer a partir de señales de respuesta inmunitaria
- Firmas de mutación del cáncer mejoran la predicción de la respuesta a inmunoterapia
- Firma inmunitaria identificada en miastenia gravis resistente al tratamiento
- Panel sindrómico permite identificación rápida de infecciones del torrente sanguíneo
- Nuevo objetivo bacteriano identificado para la detección temprana del noma
- Prueba rápida de orina acelera la selección de antibióticos para infecciones del tracto urinario
- El análisis genómico vincula cepas estreptocócicas emergentes con infecciones específicas
- La OMS respalda las pruebas rápidas en el punto de atención para mejorar la detección de tuberculosis
- Sistema integrado optimiza el flujo de trabajo preanalítico para pruebas moleculares
- Prueba de esputo no invasiva detecta el cáncer de pulmón en etapa temprana
- Nueva herramienta de IA permite seleccionar rápidamente el tratamiento en leucemia pediátrica
- Diseño innovador de espectrometría de masas podría permitir la detección de abundancias ultrabajas
- Biosensor rápido detecta la sensibilidad a fármacos en tumores de mama
- Beckman Coulter obtiene el marcado CE para un ensayo rápido que distingue infecciones bacterianas de virales
- Takara Bio USA y Hamilton se asocian para automatizar la preparación de bibliotecas NGS
- Integrated DNA Technologies se expande al ámbito del diagnóstico clínico
- Agilent Technologies adquiere la empresa de diagnóstico patológico Biocare Medical
- Cepheid se une a iniciativa del CDC para fortalecer pruebas detección de pandemias
- Encuentran etiologías de COVID prolongada en muestras de sangre con infección aguda
- Dispositivo novedoso detecta anticuerpos contra la COVID-19 en cinco minutos
- Prueba para COVID-19 mediante CRISPR detecta SARS-CoV-2 en 30 minutos usando tijeras genéticas
- Asocian disbiosis del microbioma intestinal con la COVID-19
- Validan prueba rápida novedosa de antígeno para el SARS-CoV-2 con respecto a su exactitud diagnóstica
- La IA ayuda a los clínicos con informes complejos de patología oncológica
- Herramienta de IA predice respuesta a la quimioterapia en cáncer de pulmón de células pequeñas
- Biomarcador tumoral específico predice respuesta a inmunoterapia neoadyuvante en cáncer gástrico
- Nueva prueba de IA predice resultados de quimioterapia específicos para cada paciente con cáncer de mama
- Modelo patológico basado en IA guía las decisiones de quimioterapia en cáncer de mama.



















_image.png)