Expo
ver canal
ver canal
ver canal
ver canal
ver canal
ver canal
ver canal
ver canal
Química ClínicaDiagnóstico MolecularHematologíaInmunologíaMicrobiologíaPatologíaTecnologíaIndustria
Eventos
Webinars

- Análisis de sangre rutinarios identifican biomarcadores vinculados al TEPT
- Datos proteómicos subrayan la necesidad de intervalos de referencia pediátricos específicos por edad
- Vinculan un índice del hemograma rutinario con riesgo futuro de Alzhéimer y demencia
- Biosensor rápido detecta biomarcador de cáncer de páncreas para la detección temprana
- Prueba de cribado multicáncer en orina recibe designación de dispositivo innovador de la FDA
- Un marcador genético de rutina podría ayudar a guiar la terapia dirigida en la leucemia aguda
- Panel plasmático de nueve proteínas predice la progresión de enfermedad renal en pacientes de alto riesgo
- Firma genética predice el riesgo de leucemia mieloide en el síndrome de Down
- Herramienta de predicción de riesgo mejora las pruebas genéticas para el síndrome de Li-Fraumeni
- Modelo de expresión génica guía la selección de terapia neoadyuvante en cáncer de mama
- Identifican un “interruptor protector” en el linfoma difuso de células B grandes
- Parámetros rutinarios de análisis de sangre vinculan la anemia con el riesgo de cáncer y la mortalidad
- Nuevo ensayo de función plaquetaria permite monitorizar la terapia antiplaquetaria
- Herramienta pronóstica guía el tratamiento personalizado en cáncer hematológico raro
- Plataforma abierta de multiómica identifica subtipos pronósticos en cánceres hematológicos
- Prueba de anticuerpos en sangre identifica tuberculosis activa y distingue la infección latente
- Identifican una vía inflamatoria que impulsa la resistencia a la inmunoterapia en el cáncer de vejiga
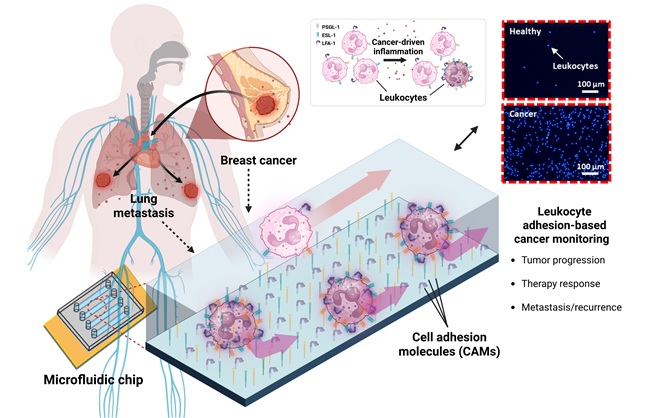
- Chip microfluídico detecta la recurrencia del cáncer a partir de señales de respuesta inmunitaria
- Firmas de mutación del cáncer mejoran la predicción de la respuesta a inmunoterapia
- Firma inmunitaria identificada en miastenia gravis resistente al tratamiento
- Panel rápido de susceptibilidad en hemocultivo amplía la cobertura para infecciones por gramnegativos
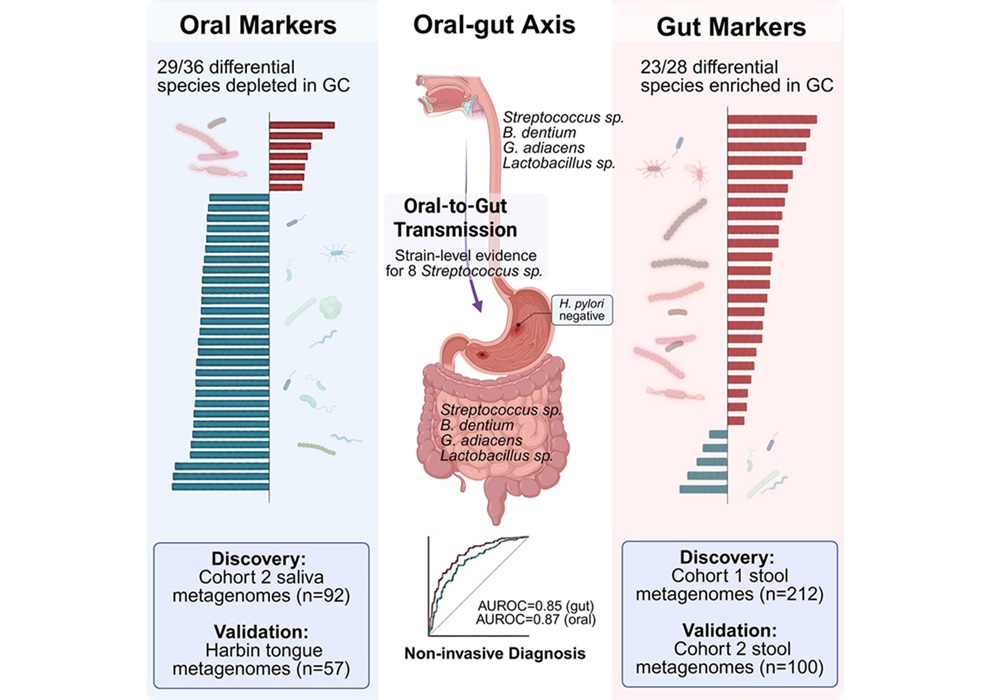
- Las características del microbioma oral e intestinal permiten identificar el cáncer gástrico temprano
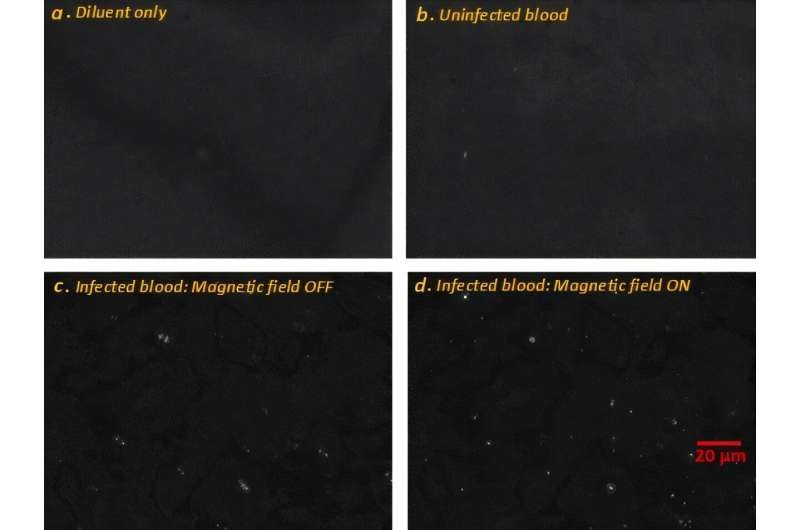
- Un método de microscopía sin marcadores permite una detección más rápida y cuantitativa de la malaria
- Prueba del microbioma intestinal predice la recurrencia del melanoma tras la cirugía
- Genes de resistencia a los antibióticos detectados en recién nacidos a las pocas horas de nacer
- Herramienta de IA predice la no respuesta a terapia dirigida en cáncer colorrectal
- Sistema integrado optimiza el flujo de trabajo preanalítico para pruebas moleculares
- Prueba de esputo no invasiva detecta el cáncer de pulmón en etapa temprana
- Nueva herramienta de IA permite seleccionar rápidamente el tratamiento en leucemia pediátrica
- Diseño innovador de espectrometría de masas podría permitir la detección de abundancias ultrabajas
- QuidelOrtho incorpora una plataforma de PCR ultrarrápida con la adquisición de LEX Diagnostics
- Una filial de Roche amplía su cartera de productos ERM con la adquisición de SAGA
- Beckman Coulter obtiene el marcado CE para un ensayo rápido que distingue infecciones bacterianas de virales
- Takara Bio USA y Hamilton se asocian para automatizar la preparación de bibliotecas NGS
- Integrated DNA Technologies se expande al ámbito del diagnóstico clínico
- Estructura inmunitaria tumoral predice respuesta a la inmunoterapia en melanoma
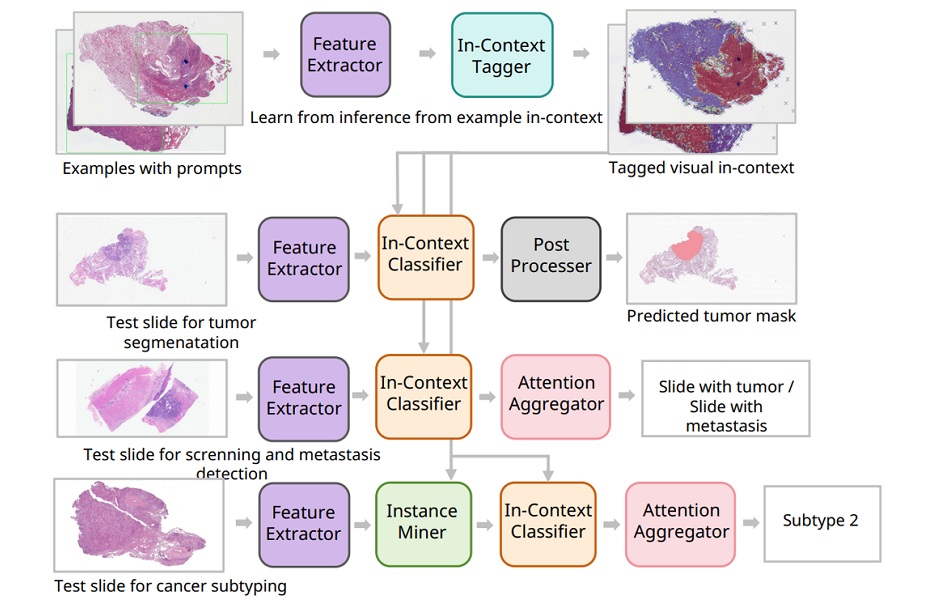
- Sistema de patología clasifica múltiples tipos de cáncer a partir de pocas muestras
- Modelo de patología con IA predice la respuesta a la inmunoterapia en cáncer de pulmón
- IA interpretable revela características celulares ocultas en imágenes de microscopía
- Ensayos basados en IA respaldan la estratificación del riesgo en cáncer de próstata y de mama

 Expo
Expo
- Análisis de sangre rutinarios identifican biomarcadores vinculados al TEPT
- Datos proteómicos subrayan la necesidad de intervalos de referencia pediátricos específicos por edad
- Vinculan un índice del hemograma rutinario con riesgo futuro de Alzhéimer y demencia
- Biosensor rápido detecta biomarcador de cáncer de páncreas para la detección temprana
- Prueba de cribado multicáncer en orina recibe designación de dispositivo innovador de la FDA
- Un marcador genético de rutina podría ayudar a guiar la terapia dirigida en la leucemia aguda
- Panel plasmático de nueve proteínas predice la progresión de enfermedad renal en pacientes de alto riesgo
- Firma genética predice el riesgo de leucemia mieloide en el síndrome de Down
- Herramienta de predicción de riesgo mejora las pruebas genéticas para el síndrome de Li-Fraumeni
- Modelo de expresión génica guía la selección de terapia neoadyuvante en cáncer de mama
- Identifican un “interruptor protector” en el linfoma difuso de células B grandes
- Parámetros rutinarios de análisis de sangre vinculan la anemia con el riesgo de cáncer y la mortalidad
- Nuevo ensayo de función plaquetaria permite monitorizar la terapia antiplaquetaria
- Herramienta pronóstica guía el tratamiento personalizado en cáncer hematológico raro
- Plataforma abierta de multiómica identifica subtipos pronósticos en cánceres hematológicos
- Prueba de anticuerpos en sangre identifica tuberculosis activa y distingue la infección latente
- Identifican una vía inflamatoria que impulsa la resistencia a la inmunoterapia en el cáncer de vejiga
- Chip microfluídico detecta la recurrencia del cáncer a partir de señales de respuesta inmunitaria
- Firmas de mutación del cáncer mejoran la predicción de la respuesta a inmunoterapia
- Firma inmunitaria identificada en miastenia gravis resistente al tratamiento
- Panel rápido de susceptibilidad en hemocultivo amplía la cobertura para infecciones por gramnegativos
- Las características del microbioma oral e intestinal permiten identificar el cáncer gástrico temprano
- Un método de microscopía sin marcadores permite una detección más rápida y cuantitativa de la malaria
- Prueba del microbioma intestinal predice la recurrencia del melanoma tras la cirugía
- Genes de resistencia a los antibióticos detectados en recién nacidos a las pocas horas de nacer
- Herramienta de IA predice la no respuesta a terapia dirigida en cáncer colorrectal
- Sistema integrado optimiza el flujo de trabajo preanalítico para pruebas moleculares
- Prueba de esputo no invasiva detecta el cáncer de pulmón en etapa temprana
- Nueva herramienta de IA permite seleccionar rápidamente el tratamiento en leucemia pediátrica
- Diseño innovador de espectrometría de masas podría permitir la detección de abundancias ultrabajas
- QuidelOrtho incorpora una plataforma de PCR ultrarrápida con la adquisición de LEX Diagnostics
- Una filial de Roche amplía su cartera de productos ERM con la adquisición de SAGA
- Beckman Coulter obtiene el marcado CE para un ensayo rápido que distingue infecciones bacterianas de virales
- Takara Bio USA y Hamilton se asocian para automatizar la preparación de bibliotecas NGS
- Integrated DNA Technologies se expande al ámbito del diagnóstico clínico
- Encuentran etiologías de COVID prolongada en muestras de sangre con infección aguda
- Dispositivo novedoso detecta anticuerpos contra la COVID-19 en cinco minutos
- Prueba para COVID-19 mediante CRISPR detecta SARS-CoV-2 en 30 minutos usando tijeras genéticas
- Asocian disbiosis del microbioma intestinal con la COVID-19
- Validan prueba rápida novedosa de antígeno para el SARS-CoV-2 con respecto a su exactitud diagnóstica
- Estructura inmunitaria tumoral predice respuesta a la inmunoterapia en melanoma
- Sistema de patología clasifica múltiples tipos de cáncer a partir de pocas muestras
- Modelo de patología con IA predice la respuesta a la inmunoterapia en cáncer de pulmón
- IA interpretable revela características celulares ocultas en imágenes de microscopía
- Ensayos basados en IA respaldan la estratificación del riesgo en cáncer de próstata y de mama














.jpg)