Expo
ver canal
ver canal
ver canal
ver canal
ver canal
ver canal
ver canal
ver canal
Química ClínicaDiagnóstico MolecularHematologíaInmunologíaMicrobiologíaPatologíaTecnología
Eventos
Webinars

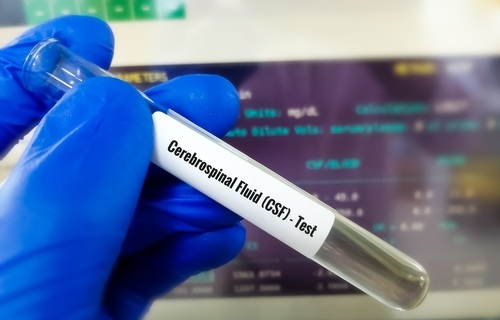
- Biomarcador en LCR mejora el diagnóstico de Parkinson y la demencia con cuerpos de Lewy
- La combinación de dos biomarcadores mejora la precisión en la detección del Alzheimer
- Nueva herramienta rastrea cambios en biomarcadores para predecir la progresión del mieloma
- Nuevo ensayo plasmático de tau mejora la predicción de la progresión del Alzheimer
- Primer inmunoensayo IVD para detectar variante genética de riesgo de Alzheimer recibe marcado CE
- Nuevo panel respiratorio amplía la detección de patógenos a 25 objetivos
- Un simple hisopado nasal podría revelar signos tempranos de la enfermedad de Alzheimer
- Biomarcador en sangre predice los resultados cognitivos tras paro cardíaco
- Análisis de sangre ayuda a orientar tratamiento en mujeres mayores con cáncer de mama
- Una biopsia líquida permite un diagnóstico más rápido del cáncer infantil en África
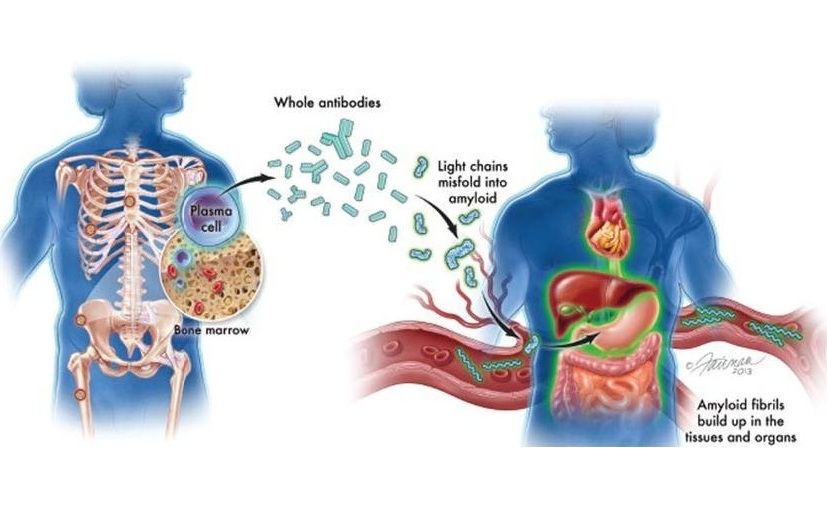
- Nuevas directrices buscan mejorar diagnóstico de amiloidosis AL
- Sistema automatizado de hemostasia ayuda a laboratorios a optimizar flujo de trabajo
- Prueba rápida y sencilla podría revolucionar transfusiones de sangre
- Análisis de sangre muy sensible mejora evaluación del riesgo de coagulación en pacientes cardíacos
- Algoritmo de IA distingue eficazmente subtipos de alfa talasemia
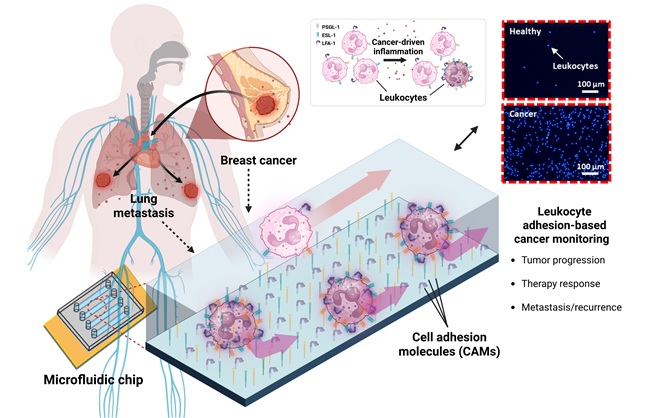
- Chip microfluídico detecta la recurrencia del cáncer a partir de señales de respuesta inmunitaria
- Firmas de mutación del cáncer mejoran la predicción de la respuesta a inmunoterapia
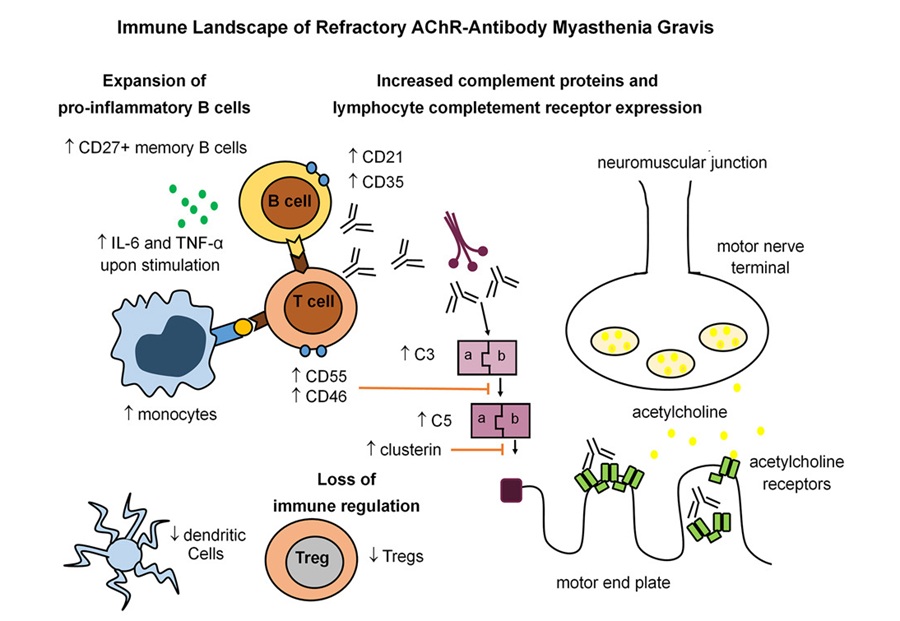
- Firma inmunitaria identificada en miastenia gravis resistente al tratamiento
- Nuevo biomarcador predice respuesta a quimioterapia en cáncer de mama triple negativo
- Análisis de sangre identifica pacientes con cáncer pulmonar beneficiarios de fármaco de inmunoterapia
- OMS recomienda pruebas POC, hisopos de lengua y agrupamiento de esputo para diagnóstico de TB
- Nuevo método de imágenes podría ayudar a predecir infecciones intestinales peligrosas
- La secuenciación rápida podría transformar la atención de la tuberculosis
- Virus intestinales ocultos vinculados al riesgo de cáncer colorrectal
- Panel de tres pruebas para detección de infecciones por duelas del hígado
- Nueva pipeta electrónica mejora flujos de trabajo con control por pantalla táctil
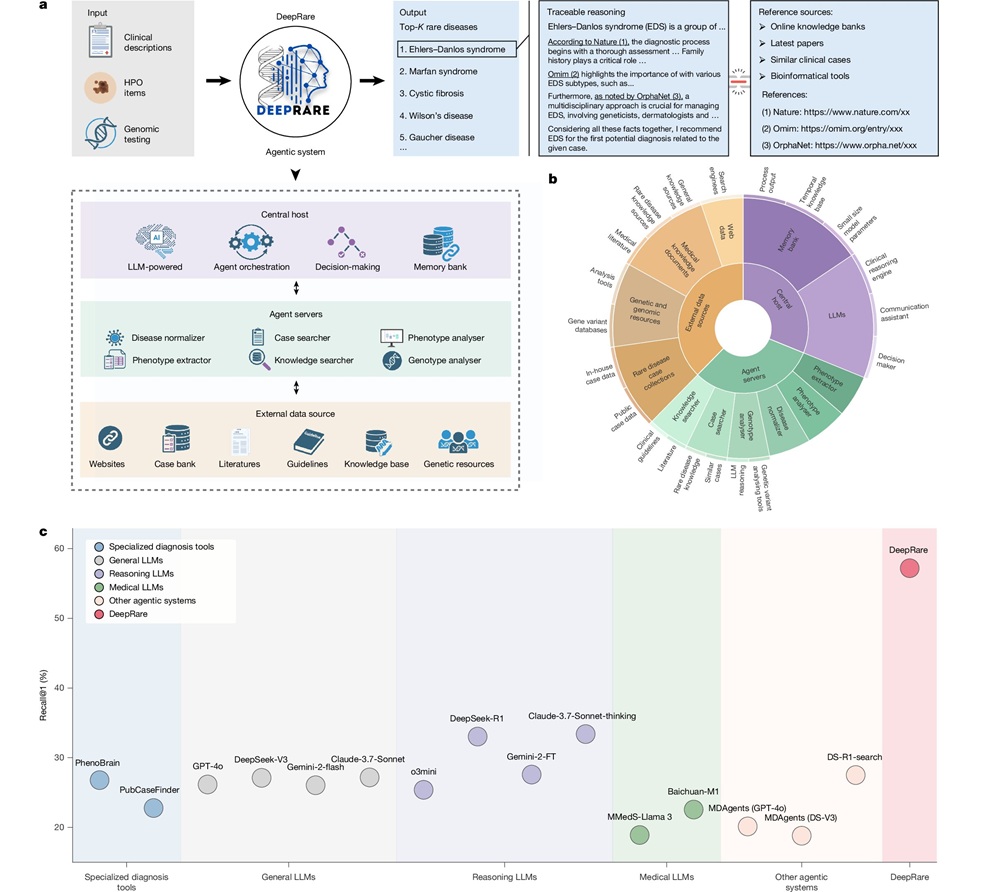
- Modelo de IA supera a clínicos en la detección de enfermedades raras
- Diagnóstico por IA demuestra alta precisión en detección de infecciones articulares periprotésicas
- “Relojes” de análisis sanguíneos predicen inicio de síntomas del Alzheimer
- Biomarcador de IA predice riesgo de cáncer de hígado
- Agilent Technologies adquiere la empresa de diagnóstico patológico Biocare Medical
- Cepheid se une a iniciativa del CDC para fortalecer pruebas detección de pandemias
- QuidelOrtho colabora con Lifotronic para ampliar cartera global de inmunoensayos
- WHX Labs en Dubái resalta habilidades de liderazgo que forman laboratorios de próxima generación
- Prueba de cáncer cervical con IA lista para lanzamiento en América Latina
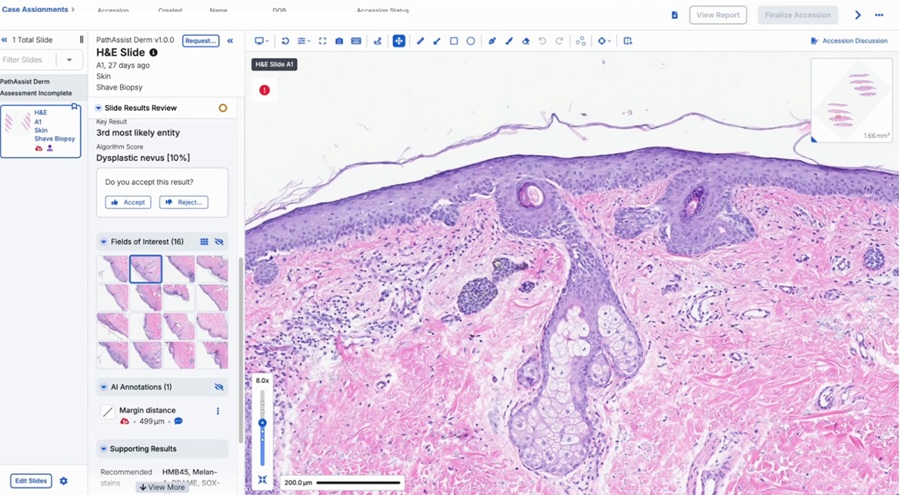
- Herramienta con IA transforma flujo de trabajo en dermatopatología
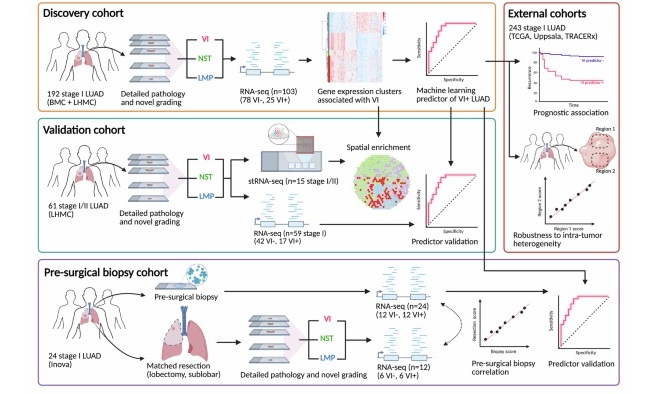
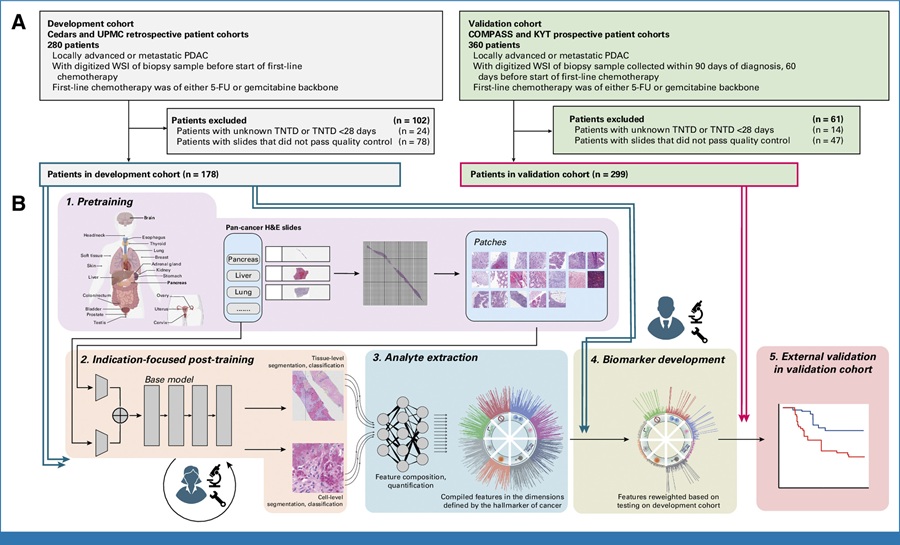
- Herramienta de IA predice la respuesta a la quimioterapia a partir de portaobjetos de biopsia
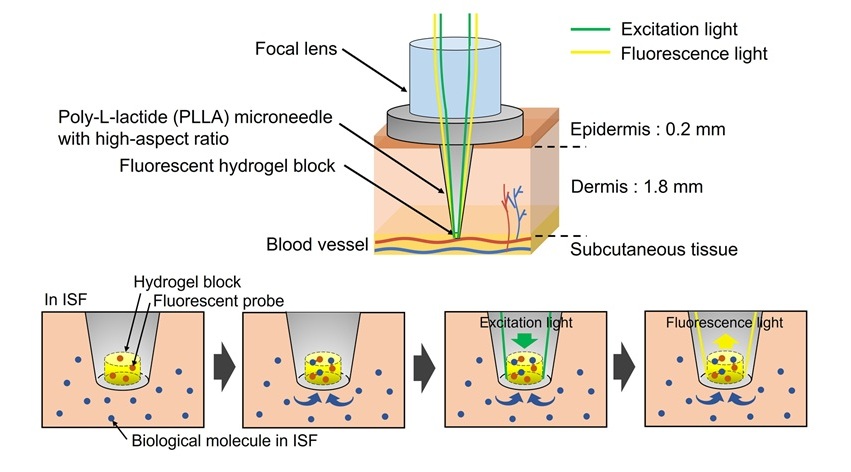
- Primer dispositivo óptico con microagujas del mundo permite pruebas clínicas sin extracción de sangre
- Nueva tecnología mcPCR podría transformar el análisis de muestras clínicas
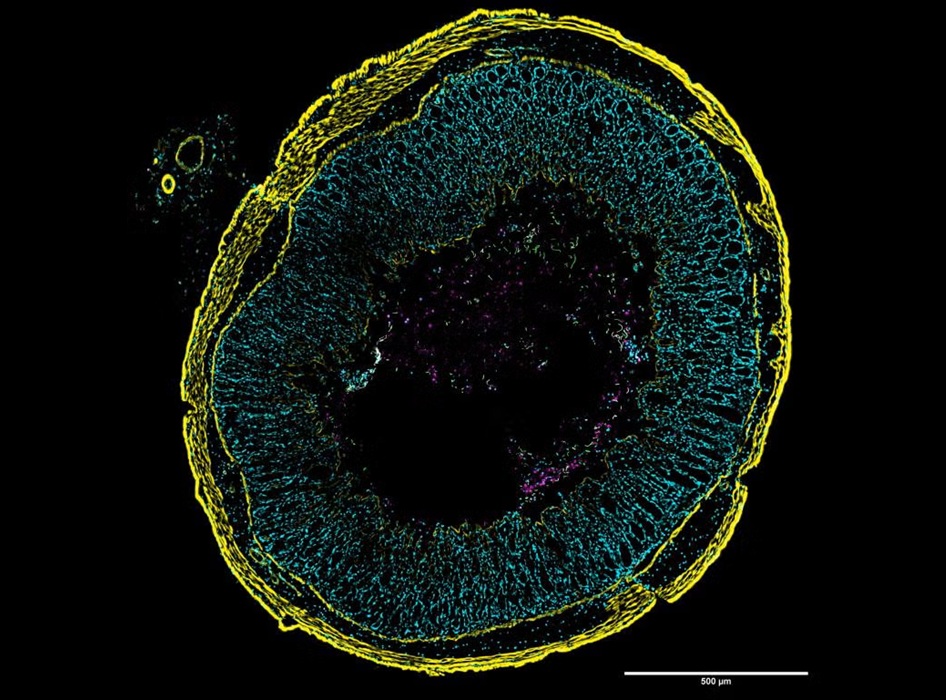
- Imágenes moleculares podrían reducir la necesidad de biopsias de melanoma

 Expo
Expo
- Biomarcador en LCR mejora el diagnóstico de Parkinson y la demencia con cuerpos de Lewy
- La combinación de dos biomarcadores mejora la precisión en la detección del Alzheimer
- Nueva herramienta rastrea cambios en biomarcadores para predecir la progresión del mieloma
- Nuevo ensayo plasmático de tau mejora la predicción de la progresión del Alzheimer
- Primer inmunoensayo IVD para detectar variante genética de riesgo de Alzheimer recibe marcado CE
- Nuevo panel respiratorio amplía la detección de patógenos a 25 objetivos
- Un simple hisopado nasal podría revelar signos tempranos de la enfermedad de Alzheimer
- Biomarcador en sangre predice los resultados cognitivos tras paro cardíaco
- Análisis de sangre ayuda a orientar tratamiento en mujeres mayores con cáncer de mama
- Una biopsia líquida permite un diagnóstico más rápido del cáncer infantil en África
- Nuevas directrices buscan mejorar diagnóstico de amiloidosis AL
- Sistema automatizado de hemostasia ayuda a laboratorios a optimizar flujo de trabajo
- Prueba rápida y sencilla podría revolucionar transfusiones de sangre
- Análisis de sangre muy sensible mejora evaluación del riesgo de coagulación en pacientes cardíacos
- Algoritmo de IA distingue eficazmente subtipos de alfa talasemia
- Chip microfluídico detecta la recurrencia del cáncer a partir de señales de respuesta inmunitaria
- Firmas de mutación del cáncer mejoran la predicción de la respuesta a inmunoterapia
- Firma inmunitaria identificada en miastenia gravis resistente al tratamiento
- Nuevo biomarcador predice respuesta a quimioterapia en cáncer de mama triple negativo
- Análisis de sangre identifica pacientes con cáncer pulmonar beneficiarios de fármaco de inmunoterapia
- OMS recomienda pruebas POC, hisopos de lengua y agrupamiento de esputo para diagnóstico de TB
- Nuevo método de imágenes podría ayudar a predecir infecciones intestinales peligrosas
- La secuenciación rápida podría transformar la atención de la tuberculosis
- Virus intestinales ocultos vinculados al riesgo de cáncer colorrectal
- Panel de tres pruebas para detección de infecciones por duelas del hígado
- Nueva pipeta electrónica mejora flujos de trabajo con control por pantalla táctil
- Modelo de IA supera a clínicos en la detección de enfermedades raras
- Diagnóstico por IA demuestra alta precisión en detección de infecciones articulares periprotésicas
- “Relojes” de análisis sanguíneos predicen inicio de síntomas del Alzheimer
- Biomarcador de IA predice riesgo de cáncer de hígado
- Agilent Technologies adquiere la empresa de diagnóstico patológico Biocare Medical
- Cepheid se une a iniciativa del CDC para fortalecer pruebas detección de pandemias
- QuidelOrtho colabora con Lifotronic para ampliar cartera global de inmunoensayos
- WHX Labs en Dubái resalta habilidades de liderazgo que forman laboratorios de próxima generación
- Prueba de cáncer cervical con IA lista para lanzamiento en América Latina
- Encuentran etiologías de COVID prolongada en muestras de sangre con infección aguda
- Dispositivo novedoso detecta anticuerpos contra la COVID-19 en cinco minutos
- Prueba para COVID-19 mediante CRISPR detecta SARS-CoV-2 en 30 minutos usando tijeras genéticas
- Asocian disbiosis del microbioma intestinal con la COVID-19
- Validan prueba rápida novedosa de antígeno para el SARS-CoV-2 con respecto a su exactitud diagnóstica
- Herramienta con IA transforma flujo de trabajo en dermatopatología
- Herramienta de IA predice la respuesta a la quimioterapia a partir de portaobjetos de biopsia
- Primer dispositivo óptico con microagujas del mundo permite pruebas clínicas sin extracción de sangre
- Nueva tecnología mcPCR podría transformar el análisis de muestras clínicas
- Imágenes moleculares podrían reducir la necesidad de biopsias de melanoma