Expo
ver canal
ver canal
ver canal
ver canal
ver canal
ver canal
ver canal
ver canal
Química ClínicaDiagnóstico MolecularHematologíaInmunologíaMicrobiologíaPatología
Industria
Eventos
Webinars

- Los análisis sanguíneos de rutina años antes del embarazo podrían identificar el riesgo de preeclampsia
- Prueba de sangre detecta cáncer testicular no identificado por marcadores estándar
- Análisis de sangre rutinarios identifican biomarcadores vinculados al TEPT
- Datos proteómicos subrayan la necesidad de intervalos de referencia pediátricos específicos por edad
- Vinculan un índice del hemograma rutinario con riesgo futuro de Alzhéimer y demencia
- Análisis de ADN en heces monitorea la actividad de la enfermedad en la EII
- Biomarcadores de biopsia líquida distinguen el cáncer de mama inflamatorio y apoyan el monitoreo
- Panel respiratorio multiplex integra extracción automatizada para agilizar las pruebas de alto volumen
- Prueba epigenética en sangre predice la respuesta a GLP-1 y monitorea los efectos del tratamiento
- Las pruebas genómicas tumorales guían la selección de inmunoterapia en tumores hipofisarios
- Identifican un “interruptor protector” en el linfoma difuso de células B grandes
- Parámetros rutinarios de análisis de sangre vinculan la anemia con el riesgo de cáncer y la mortalidad
- Nuevo ensayo de función plaquetaria permite monitorizar la terapia antiplaquetaria
- Herramienta pronóstica guía el tratamiento personalizado en cáncer hematológico raro
- Plataforma abierta de multiómica identifica subtipos pronósticos en cánceres hematológicos
- El perfil de senescencia de las células T podría predecir respuestas a la terapia CAR-T
- Prueba de flujo lateral detecta biomarcadores de sepsis en el punto de atención
- Método de cribado combinado permite identificar casos de lepra en etapas tempranas
- Prueba de anticuerpos en sangre identifica tuberculosis activa y distingue la infección latente
- Identifican una vía inflamatoria que impulsa la resistencia a la inmunoterapia en el cáncer de vejiga
- Panel rápido de susceptibilidad en hemocultivo amplía la cobertura para infecciones por gramnegativos
- Las características del microbioma oral e intestinal permiten identificar el cáncer gástrico temprano
- Un método de microscopía sin marcadores permite una detección más rápida y cuantitativa de la malaria
- Prueba del microbioma intestinal predice la recurrencia del melanoma tras la cirugía
- Genes de resistencia a los antibióticos detectados en recién nacidos a las pocas horas de nacer
- Nueva plataforma captura vesículas extracelulares para la detección temprana del cáncer
- Un ensayo microfluídico unicelular predice el riesgo de cáncer de mama
- Herramienta de IA predice la no respuesta a terapia dirigida en cáncer colorrectal
- Sistema integrado optimiza el flujo de trabajo preanalítico para pruebas moleculares
- Prueba de esputo no invasiva detecta el cáncer de pulmón en etapa temprana
- Seegene presenta plataforma de análisis de datos de PCR en tiempo real
- QuidelOrtho incorpora una plataforma de PCR ultrarrápida con la adquisición de LEX Diagnostics
- Una filial de Roche amplía su cartera de productos ERM con la adquisición de SAGA
- Beckman Coulter obtiene el marcado CE para un ensayo rápido que distingue infecciones bacterianas de virales
- Takara Bio USA y Hamilton se asocian para automatizar la preparación de bibliotecas NGS
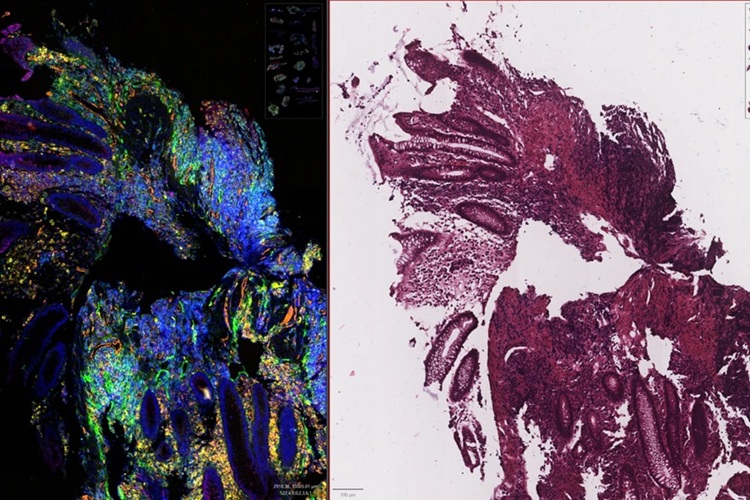
- Nueva herramienta de IA revela señales genéticas ocultas en portaobjetos H&E de rutina
- Sistema de IA analiza muestras patológicas rutinarias para predecir resultados del cáncer
- Nuevo enfoque de mapeo tisular identifica una forma de alto riesgo de enfermedad renal diabética
- Estructura inmunitaria tumoral predice respuesta a la inmunoterapia en melanoma
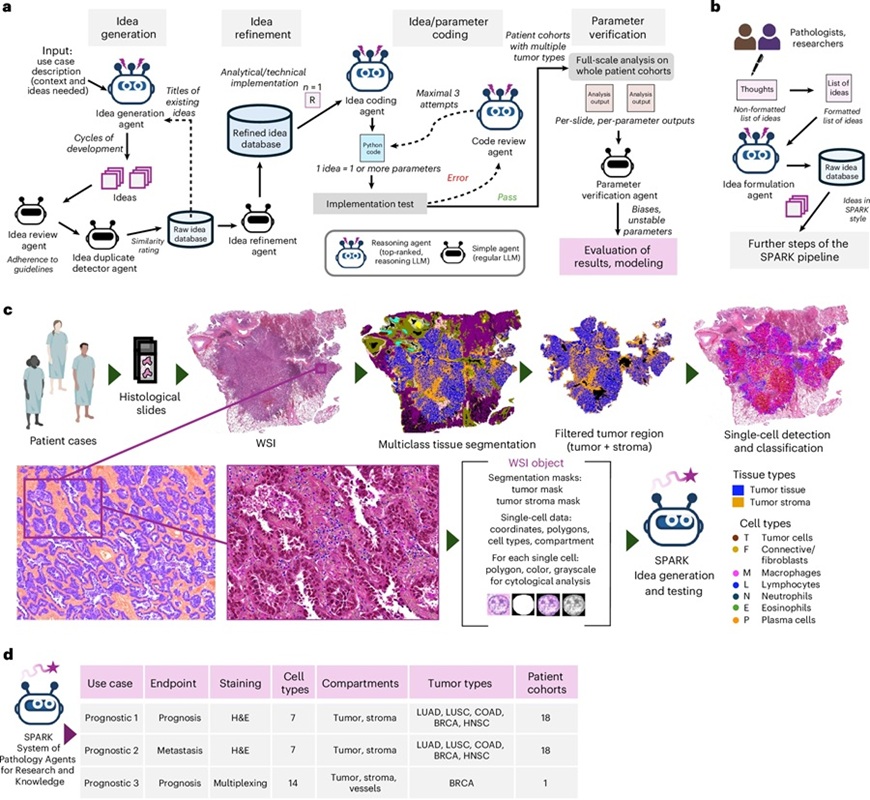
- Sistema de patología clasifica múltiples tipos de cáncer a partir de pocas muestras

 Expo
Expo
- Los análisis sanguíneos de rutina años antes del embarazo podrían identificar el riesgo de preeclampsia
- Prueba de sangre detecta cáncer testicular no identificado por marcadores estándar
- Análisis de sangre rutinarios identifican biomarcadores vinculados al TEPT
- Datos proteómicos subrayan la necesidad de intervalos de referencia pediátricos específicos por edad
- Vinculan un índice del hemograma rutinario con riesgo futuro de Alzhéimer y demencia
- Análisis de ADN en heces monitorea la actividad de la enfermedad en la EII
- Biomarcadores de biopsia líquida distinguen el cáncer de mama inflamatorio y apoyan el monitoreo
- Panel respiratorio multiplex integra extracción automatizada para agilizar las pruebas de alto volumen
- Prueba epigenética en sangre predice la respuesta a GLP-1 y monitorea los efectos del tratamiento
- Las pruebas genómicas tumorales guían la selección de inmunoterapia en tumores hipofisarios
- Identifican un “interruptor protector” en el linfoma difuso de células B grandes
- Parámetros rutinarios de análisis de sangre vinculan la anemia con el riesgo de cáncer y la mortalidad
- Nuevo ensayo de función plaquetaria permite monitorizar la terapia antiplaquetaria
- Herramienta pronóstica guía el tratamiento personalizado en cáncer hematológico raro
- Plataforma abierta de multiómica identifica subtipos pronósticos en cánceres hematológicos
- El perfil de senescencia de las células T podría predecir respuestas a la terapia CAR-T
- Prueba de flujo lateral detecta biomarcadores de sepsis en el punto de atención
- Método de cribado combinado permite identificar casos de lepra en etapas tempranas
- Prueba de anticuerpos en sangre identifica tuberculosis activa y distingue la infección latente
- Identifican una vía inflamatoria que impulsa la resistencia a la inmunoterapia en el cáncer de vejiga
- Panel rápido de susceptibilidad en hemocultivo amplía la cobertura para infecciones por gramnegativos
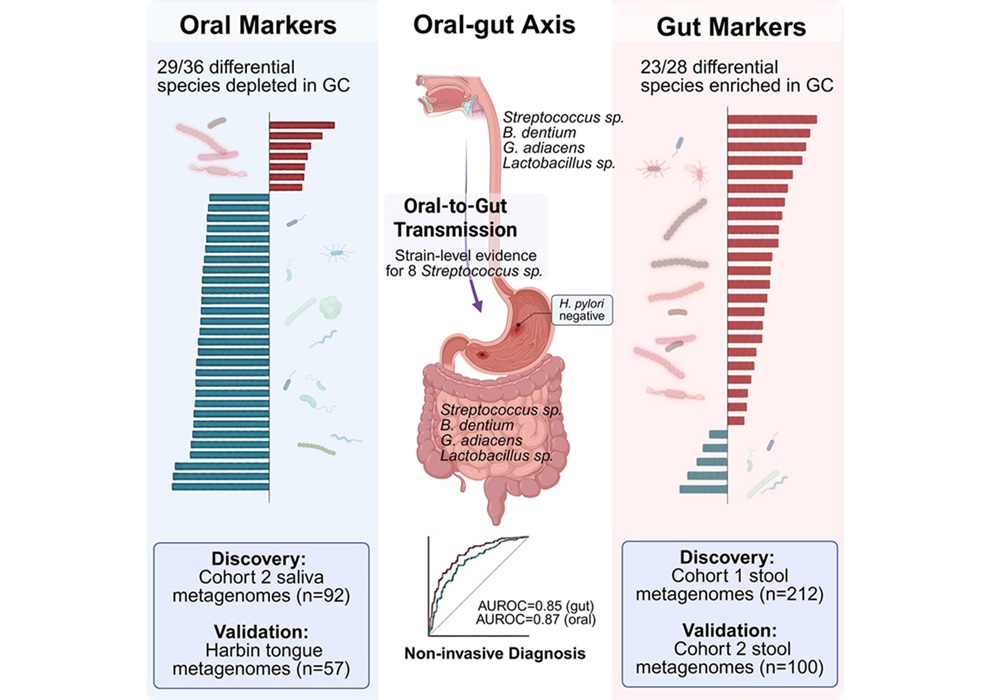
- Las características del microbioma oral e intestinal permiten identificar el cáncer gástrico temprano
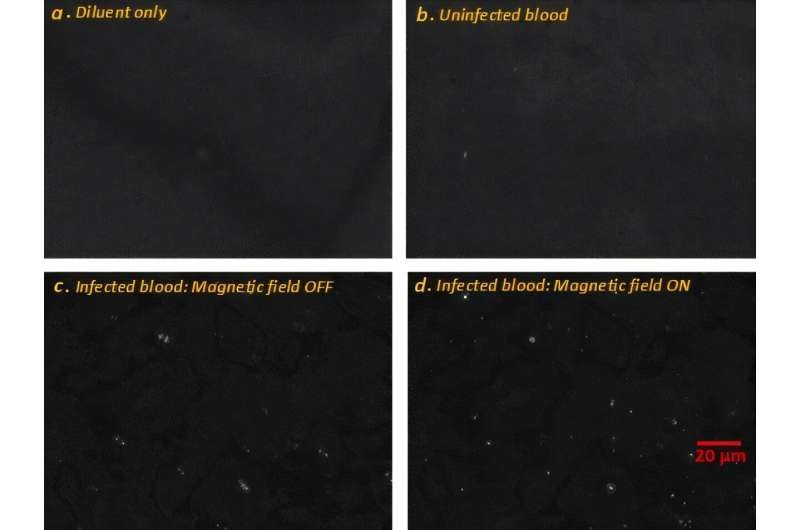
- Un método de microscopía sin marcadores permite una detección más rápida y cuantitativa de la malaria
- Prueba del microbioma intestinal predice la recurrencia del melanoma tras la cirugía
- Genes de resistencia a los antibióticos detectados en recién nacidos a las pocas horas de nacer
- Nueva plataforma captura vesículas extracelulares para la detección temprana del cáncer
- Un ensayo microfluídico unicelular predice el riesgo de cáncer de mama
- Herramienta de IA predice la no respuesta a terapia dirigida en cáncer colorrectal
- Sistema integrado optimiza el flujo de trabajo preanalítico para pruebas moleculares
- Prueba de esputo no invasiva detecta el cáncer de pulmón en etapa temprana
- Seegene presenta plataforma de análisis de datos de PCR en tiempo real
- QuidelOrtho incorpora una plataforma de PCR ultrarrápida con la adquisición de LEX Diagnostics
- Una filial de Roche amplía su cartera de productos ERM con la adquisición de SAGA
- Beckman Coulter obtiene el marcado CE para un ensayo rápido que distingue infecciones bacterianas de virales
- Takara Bio USA y Hamilton se asocian para automatizar la preparación de bibliotecas NGS
- Encuentran etiologías de COVID prolongada en muestras de sangre con infección aguda
- Dispositivo novedoso detecta anticuerpos contra la COVID-19 en cinco minutos
- Prueba para COVID-19 mediante CRISPR detecta SARS-CoV-2 en 30 minutos usando tijeras genéticas
- Asocian disbiosis del microbioma intestinal con la COVID-19
- Validan prueba rápida novedosa de antígeno para el SARS-CoV-2 con respecto a su exactitud diagnóstica
- Nueva herramienta de IA revela señales genéticas ocultas en portaobjetos H&E de rutina
- Sistema de IA analiza muestras patológicas rutinarias para predecir resultados del cáncer
- Nuevo enfoque de mapeo tisular identifica una forma de alto riesgo de enfermedad renal diabética
- Estructura inmunitaria tumoral predice respuesta a la inmunoterapia en melanoma
- Sistema de patología clasifica múltiples tipos de cáncer a partir de pocas muestras