Expo
ver canal
ver canal
ver canal
ver canal
ver canal
ver canal
ver canal
ver canal
Química ClínicaDiagnóstico MolecularHematologíaInmunologíaMicrobiología
TecnologíaIndustria
Eventos
Webinars

- Prueba de orina para Alzheimer recibe designación de dispositivo innovador de la FDA
- Un sensor basado en sangre detecta los primeros signos de Alzheimer y Parkinson
- Biomarcadores de biopsia líquida podrían mejorar el diagnóstico de la epilepsia infantil
- Biomarcador en líquido mejora el diagnóstico y monitoreo del linfoma primario del SNC
- Nuevo valor de corte de CA19-9 ayuda a identificar pacientes con cáncer de páncreas de alto riesgo
- Marcadores proteicos en sangre detectan riesgo de esclerosis múltiple años antes del diagnóstico
- Prueba genómica predice beneficio de quimioterapia en cáncer de próstata metastásico
- Ensayos de PCR digital apoyan la vigilancia de brote de ebolavirus Bundibugyo
- Declaraciones de postura describen estándares de evidencia para pruebas de detección multicáncer
- Prueba sanguínea ultrasensible de MRD detecta recurrencia temprana del cáncer de mama
- El recuento de eosinófilos en sangre podría predecir la respuesta y toxicidad a inmunoterapia oncológica
- Un umbral de ferritina más elevado podría mejorar la detección de deficiencia de hierro en niños
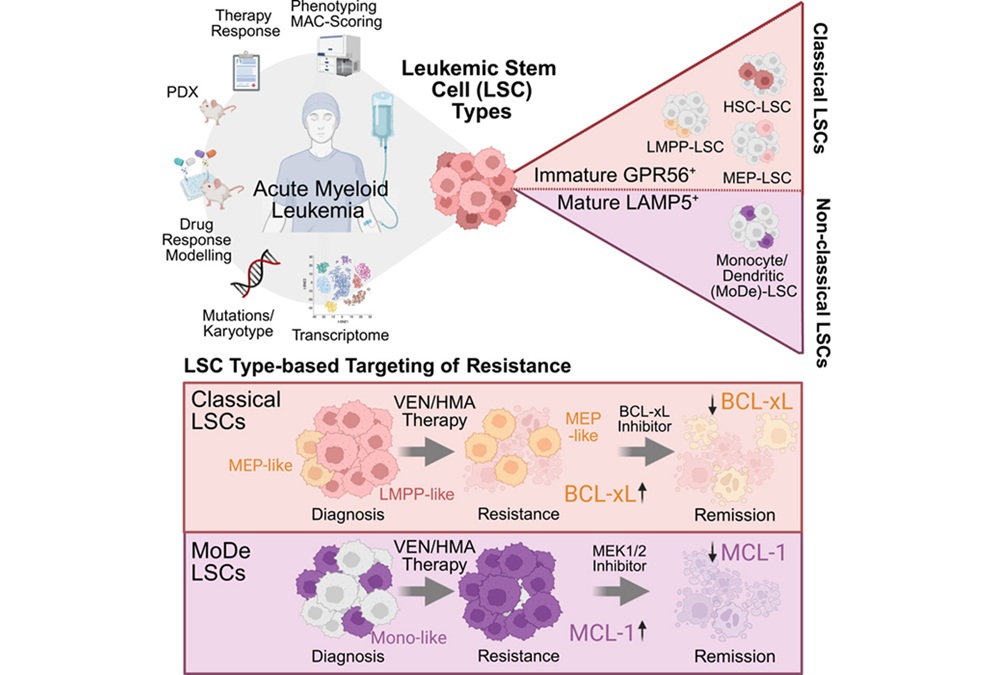
- Los biomarcadores de células madre podrían orientar el tratamiento en la leucemia mieloide aguda
- Análisis de sangre permite la detección temprana de recaída del mieloma múltiple
- Identifican un “interruptor protector” en el linfoma difuso de células B grandes
- Un estudio apunta a vía autoinmune detrás de síntomas de COVID prolongado
- Enzima inmunitaria se vincula con la enfermedad inflamatoria intestinal resistente al tratamiento
- Análisis de sangre simple podría reemplazar biopsias para monitorizar el rechazo del trasplante pulmonar
- Una prueba rutinaria de cribado de tuberculosis podría revelar el envejecimiento inmunológico
- Las pruebas en el punto de atención podrían ampliar el acceso al diagnóstico de Mpox
- Un panel gastrointestinal aprobado por la FDA detecta 24 patógenos
- Nuevo ensayo de RAM respalda el cribado rápido para el control de infecciones en hospitales
- Estudio revela que infecciones ocultas de mpox podrían impulsar su propagación continua
- Vigilancia genómica a gran escala rastrea bacterias resistentes en hospitales europeos
- Biosensor de antígeno detecta tuberculosis activa en una hora
- Los kits de detección enviados por correo ayudan a reducir brechas en el cribado del cáncer colorrectal
- Flujo de trabajo totalmente automatizado de muestra a resultado impulsa las pruebas de TB latente
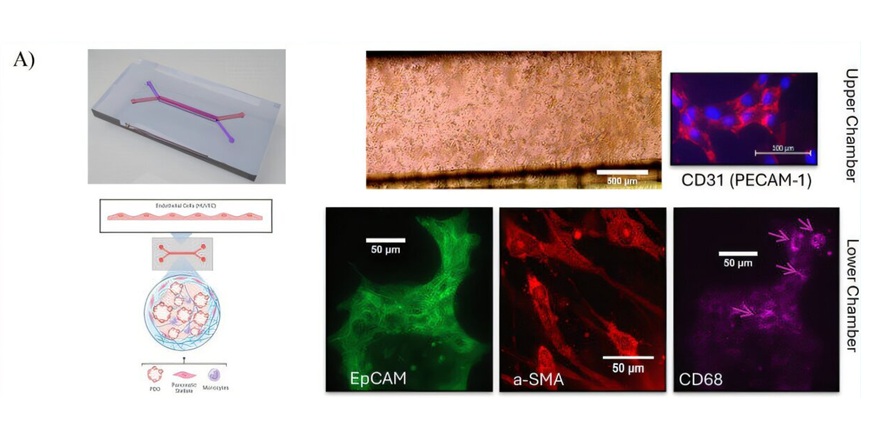
- Plataforma de 'tumor en un chip' modela la respuesta al tratamiento del cáncer de páncreas
- Nueva plataforma captura vesículas extracelulares para la detección temprana del cáncer
- Un ensayo microfluídico unicelular predice el riesgo de cáncer de mama
- Fujifilm integra informes estructurados en el flujo de trabajo de patología digital
- Analizador multifuncional impulsado por IA gana el Premio Alemán de Innovación
- Roche adquirirá PathAI por hasta 1.050 millones de dólares para fortalecer su cartera de diagnósticos con IA
- Seegene presenta plataforma de análisis de datos de PCR en tiempo real
- QuidelOrtho incorpora una plataforma de PCR ultrarrápida con la adquisición de LEX Diagnostics
- Herramienta de IA extrae señales inmunitarias de biopsias para orientar la terapia del mieloma
- Prueba de patología con IA recibe designación de avance de la FDA para riesgo de cáncer de vejiga
- Herramienta de IA predice la expresión génica espacial del cáncer a partir de imágenes de patología
- Herramienta de patología digital con IA para la estratificación del riesgo en cáncer de mama
- Nueva herramienta de IA revela señales genéticas ocultas en portaobjetos H&E de rutina

 Expo
Expo
- Prueba de orina para Alzheimer recibe designación de dispositivo innovador de la FDA
- Un sensor basado en sangre detecta los primeros signos de Alzheimer y Parkinson
- Biomarcadores de biopsia líquida podrían mejorar el diagnóstico de la epilepsia infantil
- Biomarcador en líquido mejora el diagnóstico y monitoreo del linfoma primario del SNC
- Nuevo valor de corte de CA19-9 ayuda a identificar pacientes con cáncer de páncreas de alto riesgo
- Marcadores proteicos en sangre detectan riesgo de esclerosis múltiple años antes del diagnóstico
- Prueba genómica predice beneficio de quimioterapia en cáncer de próstata metastásico
- Ensayos de PCR digital apoyan la vigilancia de brote de ebolavirus Bundibugyo
- Declaraciones de postura describen estándares de evidencia para pruebas de detección multicáncer
- Prueba sanguínea ultrasensible de MRD detecta recurrencia temprana del cáncer de mama
- El recuento de eosinófilos en sangre podría predecir la respuesta y toxicidad a inmunoterapia oncológica
- Un umbral de ferritina más elevado podría mejorar la detección de deficiencia de hierro en niños
- Los biomarcadores de células madre podrían orientar el tratamiento en la leucemia mieloide aguda
- Análisis de sangre permite la detección temprana de recaída del mieloma múltiple
- Identifican un “interruptor protector” en el linfoma difuso de células B grandes
- Un estudio apunta a vía autoinmune detrás de síntomas de COVID prolongado
- Enzima inmunitaria se vincula con la enfermedad inflamatoria intestinal resistente al tratamiento
- Análisis de sangre simple podría reemplazar biopsias para monitorizar el rechazo del trasplante pulmonar
- Una prueba rutinaria de cribado de tuberculosis podría revelar el envejecimiento inmunológico
- Las pruebas en el punto de atención podrían ampliar el acceso al diagnóstico de Mpox
- Un panel gastrointestinal aprobado por la FDA detecta 24 patógenos
- Nuevo ensayo de RAM respalda el cribado rápido para el control de infecciones en hospitales
- Estudio revela que infecciones ocultas de mpox podrían impulsar su propagación continua
- Vigilancia genómica a gran escala rastrea bacterias resistentes en hospitales europeos
- Biosensor de antígeno detecta tuberculosis activa en una hora
- Los kits de detección enviados por correo ayudan a reducir brechas en el cribado del cáncer colorrectal
- Flujo de trabajo totalmente automatizado de muestra a resultado impulsa las pruebas de TB latente
- Plataforma de 'tumor en un chip' modela la respuesta al tratamiento del cáncer de páncreas
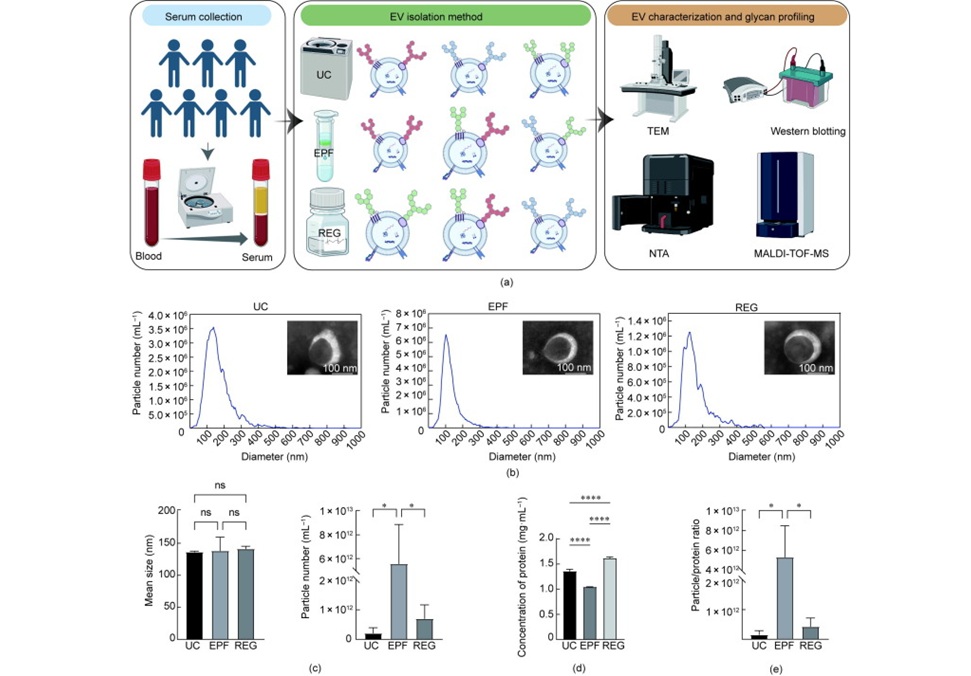
- Nueva plataforma captura vesículas extracelulares para la detección temprana del cáncer
- Un ensayo microfluídico unicelular predice el riesgo de cáncer de mama
- Fujifilm integra informes estructurados en el flujo de trabajo de patología digital
- Analizador multifuncional impulsado por IA gana el Premio Alemán de Innovación
- Roche adquirirá PathAI por hasta 1.050 millones de dólares para fortalecer su cartera de diagnósticos con IA
- Seegene presenta plataforma de análisis de datos de PCR en tiempo real
- QuidelOrtho incorpora una plataforma de PCR ultrarrápida con la adquisición de LEX Diagnostics
- Encuentran etiologías de COVID prolongada en muestras de sangre con infección aguda
- Dispositivo novedoso detecta anticuerpos contra la COVID-19 en cinco minutos
- Prueba para COVID-19 mediante CRISPR detecta SARS-CoV-2 en 30 minutos usando tijeras genéticas
- Asocian disbiosis del microbioma intestinal con la COVID-19
- Validan prueba rápida novedosa de antígeno para el SARS-CoV-2 con respecto a su exactitud diagnóstica
- Herramienta de IA extrae señales inmunitarias de biopsias para orientar la terapia del mieloma
- Prueba de patología con IA recibe designación de avance de la FDA para riesgo de cáncer de vejiga
- Herramienta de IA predice la expresión génica espacial del cáncer a partir de imágenes de patología
- Herramienta de patología digital con IA para la estratificación del riesgo en cáncer de mama
- Nueva herramienta de IA revela señales genéticas ocultas en portaobjetos H&E de rutina